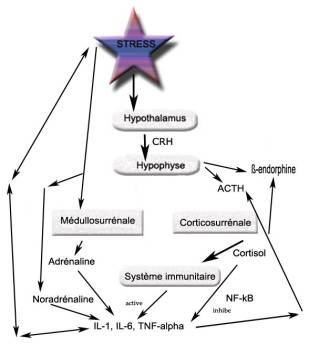
Résumé : La neuropathie périphérique chimio-induite (NPCI), définie par des dommages du système nerveux périphérique engendrés par les agents anticancéreux engendre des troubles à type de douleurs neuropathiques, des symptômes moteurs mais aussi des troubles trophiques. La douleur neuropathique résulte d’un mécanisme de sensibilisation périphérique et centrale. Comme le montrent les nombreuses études acupuncturales expérimentales sur modèle animal de neuropathie, le contrôle de la douleur peut s’effectuer par modulation de différentes molécules comme l’adénosine, la substance P, les peptides opioïdes endogènes, les récepteurs vanilloïdes 1 (TRPV1), le calcitonin gene-related peptide (CGRP), les récepteurs glutamiques NMDA, les cytokines pro-inflammatoires TNF-α, IL-6, IL-1β, les métalloprotéases matricielles MMP-9 et MMP-2, les prostaglandine E2 (PGE2), les dérivés réactifs de l’oxygène (reactive oxygen species, ROS) etc. Mots-clés : douleur neuropathique – neuropathie périphérique chimio-induite – acupuncture – sensibilisation périphérique et centrale.
Summary: Chemotherapy-induced peripheral neuropathy (CIPN), defined by peripheral nervous system damage caused by anticancer agents leads to disorders as neuropathic pain, motor symptoms but also trophic disorders. Neuropathic pain results from a peripheral and central sensitization mechanism. As shown in many experimental studies in acupuncture using animal model of neuropathy, pain control may be performed by modulation of different molecules such as adenosine, substance P, endogenous opioid peptides, vanilloid receptor 1 (TRPV1), calcitonin gene-related peptide ( CGRP), glutamic NMDA receptors, pro-inflammatory cytokines TNF-α , IL-6, IL-1β , matrix metalloproteinases MMP-9 and MMP-2, prostaglandin E2 (PGE2), reactive oxygen species (reactive oxygen species, ROS..). Keywords: Neuropathic Pain – chemotherapy-induced peripheral neuropathy – acupuncture – peripheral and central sensitization.

La neuropathie périphérique chimio-induite (NPCI) est définie par des dommages du système nerveux périphérique engendrés par les agents anticancéreux comme les sels de platine (oxaliplatine, carboplatine, cisplatine), les taxanes (paclitaxel, docétaxel, cabazitaxel) et épothilone, les alcaloïdes de la pervenche (les vinca-alcaloïdes : vincristine, vinblastine, vinorelbine, vindésine), la bortézomib, l’éribuline, la thalidomide et la lénalidomide, la doxorubicine [1-4]. Ces neuropathies se distinguent par la symétrie des troubles neurologiques et leur prédominance distale sans aucune systématisation tronculaire ou radiculaire. L’atteinte porte sur les divers types de fibres sensitives, motrices et végétatives. Cependant, la plupart des symptômes de la NPCI correspondent à un tableau clinique de polyneuropathie sensitive engendrant perte de sensibilité, paresthésies, dysesthésies, sensations de brûlures. Des symptômes moteurs comme les crampes, les fasciculations, l’amyotrophie mais aussi des troubles trophiques peuvent être également retrouvés. Cela affecte essentiellement une distribution à progression distale vers les orteils et les doigts (figure 1) correspondant au syndrome mains-pieds, mais peut aussi toucher la région péribuccale ou la face.
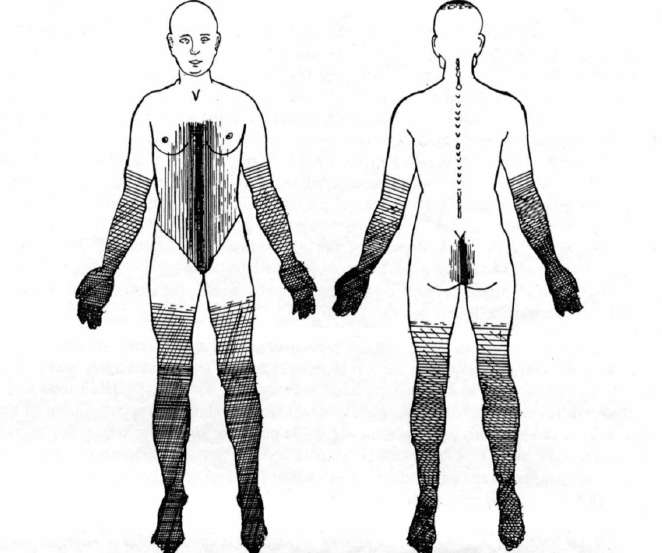
Figure 1. Répartition de l’atteinte thermoalgique dans les polyneuropathies axonales ascendantes progressives [[5]].
En outre, la NPCI chez la plupart des patients n’est que partiellement réversible et peut persister longtemps après que la chimiothérapie soit achevée [[6]]. C’est un des effets indésirables dose-limitant majeurs de la chimiothérapie pouvant conduire non seulement à la perte de la fonction physique associée à une diminution de la qualité de vie et des difficultés dans les activités quotidiennes, mais pouvant également entraîner la réduction et/ou retarder la dose d’administration, voire même dans le pire des cas l’arrêt de la thérapeutique anticancéreuse [[7]].
Physiopathologie de la neurotoxicité
Le mécanisme de la neurotoxicité des agents anticancéreux commence à être mieux connu. La neuropathie peut résulter de diverses causes : atteinte du transport médié par des microtubules au niveau des axones ; dégénérescence axonale distale [[8]] ; changement morphologique des noyaux des neurones des ganglions rachidiens de la racine dorsale (GRD) ; altération du fonctionnement des mitochondries dans les axones, accumulation intra-axonale du sodium et du calcium du fait de la perturbation des canaux ioniques voltage-dépendants sodium/potassium [2,9]]. L’atteinte neurotoxique dépend du type de chimiothérapie (figure 2). Ainsi chez des rats traités à la vincristine, on observera une atteinte du transport axonal rétrograde des fibres myélinisées non nociceptives Aβ. L’oxaliplatine engendre des atteintes des noyaux des neurones des GRD, des canalopathies du canal sodique Nav, mais aussi des récepteurs thermiques au froid de la famille des transient receptor potential (TRP : TRPM8 et TRPA1). Le paclitaxel engendre quant à lui une altération du fonctionnement mitochondrial des axones mais aussi des canaux calciques.
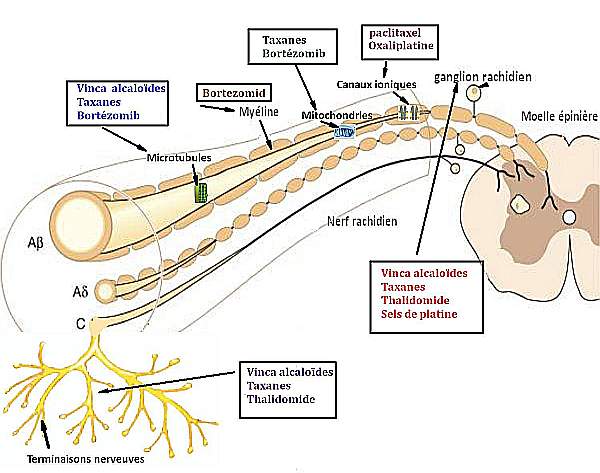
Figure 2. Les principaux effets neurotoxiques des chimiothérapies selon l’apport des modèles expérimentaux [2,3,9].
Physiopathologie de la douleur neuropathique
La douleur nociceptive survient lorsqu’en périphérie, il y a un excès de stimuli intenses aigus (plaie, traumatisme, brûlure, lésion etc.), voire chroniques comme les rhumatismes ou le cancer. Le message douloureux engendré par les nocicepteurs est transmis par les voies sensitives extra-lemniscales jusqu’au cortex cérébral, provoquant alors sa perception localisée au territoire atteint. A l’inverse, la douleur neuropathique (encore appelée de désafférentation) est très souvent chronique et résulte d’une lésion ou d’une irritation de l’un des éléments constitutifs, périphériques (amputation avec syndrome du membre fantôme, section, zona, cancer) et/ou central (accident vasculaire cérébral) des voies nociceptives. Il survient des dysfonctionnements des voies nociceptives qui génèrent des sensations anormales sensitives ressenties comme douloureuses (paresthésies, dysesthésies, allodynie, hyperalgésie…) et tout cela en l’absence de dégât tissulaire apparent.
Le développement de la douleur neuropathique implique donc non seulement les voies neuronales, mais aussi les cellules de Schwann et les neurones des ganglions rachidiens de la racine dorsale, les composants du système immunitaire périphérique, la microglie et les astrocytes. La douleur neuropathique a de nombreuses caractéristiques d’un trouble neuroimmunologique avec trouble des voies de signalisation réciproques entre les cellules neuronales et non-neuronales [[10]].
Sensibilisation périphérique
La douleur chronique (qu’elle soit inflammatoire ou/et neuropathique) est censée être causée par une réponse neuronale aberrante le long de la voie de transmission de la douleur du ganglion de la racine dorsale (DRG) à la moelle épinière puis au thalamus et au cortex. Des origines à la fois centrale et périphérique sont susceptibles d’être impliquées dans la douleur chronique. Après une lésion tissulaire, on aura la sensibilisation des nocicepteurs par une «soupe » inflammatoire qui conduit à l’hyperalgésie primaire et la douleur inflammatoire. Il s’agit de la sensibilisation périphérique.
Les terminaisons libres des nocicepteurs C ou Aδ sont activées. De nombreux récepteurs biochimiques sont impliqués : les récepteurs ionotropiques pour le sodium ou le calcium, les récepteurs vanilloïdes VR1 ou transient receptor potential vanilloid TRPV1 (sensibles à la chaleur), les récepteurs à l’acidité (ASIC) et les récepteurs purinergiques de type P2X (adénosine triphosphate, ATP). En plus de réagir à certaines variations mécaniques et thermiques, la majorité des nocicepteurs se comportent comme des chémorécepteurs.
La « soupe » inflammatoire comprend diverses substances algogènes. Elles peuvent être formées localement ou être des substances circulantes, dont l’action est facilitée par la fréquente contiguïté des terminaisons A et C avec les artérioles ou des veinules. On objective les ions H+, K+ et ATP en rapport avec les cellules lésées ; les cytokines pro-inflammatoires (interleukines IL-1β, IL-6, IL-8 et TNF-α) et neurotrophines (facteur de croissance : Nerve Growth Factor – NGF, brain-derivated neurotrophic factor – BDNF) issues des cellules inflammatoires locales (macrophages) ; la bradykinine à partir des kininogènes plasmatiques. L’histamine provient des mastocytes, la sérotonine des plaquettes ; les peptides (substance P, le calcitonin gene-related peptide (CGRP), neurokine A, glutamate) sont libérés par les nocicepteurs eux-mêmes et les prostaglandines comme la PGE2 issues de l’acide arachidonique sous l’action de la cyclo-oxygénase 2 (COX-2). Ainsi, par une cascade de réactions auto-entretenues, ces différentes substances interagissent entre elles avec activation des nocicepteurs, vasodilatation et inflammation entraînant l’inflammation neurogène par le phénomème du réflexe d’axone [[11]].
Sensibilisation centrale par hyperexcitabilité des neurones
La transmission de la douleur se réalise vers la première synapse dans la moelle. Les lésions nerveuses induisent de profondes modifications métaboliques au niveau des corps cellulaires des neurones afférents primaires localisés dans les ganglions rachidiens. Ces modifications se traduisent par une réduction (comme ceux des récepteurs morphiniques) ou une augmentation de la libération de divers neuropeptides (substance P, CGRP, VIP, etc.). Ont été aussi décrits de véritables transformations des fibres de gros calibres (fibres A), véhiculant normalement les messages non nociceptifs, qui se comportent comme des nocicepteurs (les fibres type C ou A) et synthétisent même des neuropeptides pronociceptifs tels que la substance P ou le BDNF, élément clé de la sensibilisation centrale [[12,23]. Une hyperexcitabilité périphérique sous l’effet direct des lésions des fibres périphériques pourra être observée avec remaniements des canaux ioniques qui règlent l’excitabilité membranaire, comme les canaux potassiques. Les récepteurs de la famille TRP interviendraient aussi.
Les neurones spinaux situés dans les couches superficielles et profondes de la corne dorsale de la moelle sont activés par les fibres afférentes nociceptives (Aδ et C). La transmission des messages nociceptifs périphériques vers les neurones spinaux est réalisée par deux groupes principaux de substances : les acides aminés excitateurs comme le glutamate et les neuropeptides qui modulent les effets des premiers. Leur libération, par exocytose des vésicules synaptiques est déclenchée par le calcium cytosolique des terminaisons des fibres afférentes primaires. Plus d’une vingtaine de substances sont ainsi libérées par la fibre présynaptique. On retrouve : la substance P, le calcitonine gene-related peptide (CGRP), la somatostatine, la cholécystokinine (CCK), le neuropeptide FF, la neurokinine A…
Au niveau présynaptique, il existe d’autres mécanismes susceptibles de favoriser ou d’inhiber la libération des neuromédiateurs par l’intermédiaire de récepteurs spécifiques. Les mécanismes favorisant leur libération sont constitués de l’ATP (avec les récepteurs P2X), de la sérotonine (avec les récepteurs 5-HT3) et des prostaglandines (avec les récepteurs EP). Leur inhibition est réalisée par les opioïdes (avec les récepteurs morphiniques essentiellement μ, à un moindre degré δ et très faiblement κ), de la sérotonine (récepteurs 5-HT1A et 5-HT1B), de la noradrénaline (récepteurs α2), de l’acide gamma-aminobutyrique (GABA) (avec les récepteurs GABAB) [12], de l’acétylcholine (récepteurs nicotiniques ou muscariniques [13-16].
La potentialisation à long terme (LTP)
Les mécanismes de sensibilisation centrale sont quasi semblables pour les différents types de douleurs, qu’elles soient inflammatoires ou neuropathiques. La sensibilisation centrale débute avec une cascade d’événements dans la corne postérieure de la moelle. La libération excessive de neuromédiateurs par la fibre présynaptique aboutit à une augmentation importante de la transmission de la douleur. Le système des récepteurs au glutamate NMDA joue un rôle central dans les phénomènes d’hyperalgie. À l’état basal, le récepteur NMDA est inactif, seuls les récepteurs ionotropiques AMPA s’activent sous l’effet du glutamate.
Des activités ectopiques spontanées ou un stimulus nociceptif intense et répété (phénomène d’embrasement dit « wind-up ») ou prolongé conduit à une augmentation disproportionnée des réponses dans la corne postérieure avec dépolarisation du neurone qui ouvre le canal ionique associé à la sous-unité NR2B des récepteurs NMDA enclenchant une entrée massive de calcium dans la cellule. De récents travaux montrent que la forte concentration de calcium intracellulaire active la NO synthase, source de production de monoxyde d’azote (oxyde nitrique NO) intracellulaire et la cyclooxygénase de type 2 (COX 2) à l’origine de la synthèse de prostaglandines centrales. Le NO et les prostaglandines peuvent diffuser dans les éléments présynaptiques ou dans les cellules gliales, et par ce mécanisme être à l’origine d’une augmentation de la libération présynaptique de glutamate, contribuant au développement d’une hyperexcitabilité centrale. Par ailleurs, les prostaglandines vont inhiber les interneurones inhibiteurs ayant pour médiateur le GABA. L’altération de l’inhibition GABA dans la corne postérieure va contribuer aussi à la douleur neuropathique.
Le NO et le calcium interviennent également en modifiant l’expression de certains gènes, dont les gènes dits à expression immédiate (c-FOS, c-JUN, CREB, Egr 1…) et à réponse tardive comme les gènes codant notamment pour la prodynorphine, les récepteurs de la substance P et de la neurokinine A (récepteurs NK1, NK2), des neurotrophines tel que le BDNF… Ces protéines ainsi synthétisées sont responsables de la potentialisation cellulaire à long terme à l’origine de la neuroplasticité centrale pouvant expliquer le passage à la chronicité avec douleurs de type neuropathique par phénomènes de mémorisation de la douleur [12,17-19].
Cytokines et mécanismes au niveau de la microglie
En outre, d’autres mécanismes sont impliqués dans la sensibilisation centrale par interactions neuro-immunes, médiées par les cytokines et les cellules gliales. Normalement, en cas de douleur aigue nociceptive, les astrocytes et la microglie ne sont pas activés mais le seront en cas de douleur de type neuropathique. Les cellules gliales peuvent être activées par différentes substances comme les acides aminés excitateurs, la substance P, le glutamate, le NO, les prostaglandines et l’ATP. Les cellules gliales sont des cellules immunologiquement compétentes, susceptibles de libérer du NO et des cytokines pro-inflammatoires comme l’IL-1β, l’IL-6 et le facteur de nécrose tumorale alpha (TNF-α). Ces substances vont participer à majorer encore la réponse douloureuse. La neuro-inflammation donne lieu à une « activation » des astrocytes et de la microglie, marquée par la production accrue de certains marqueurs intracellulaires, dont la protéine fibrillaire acide. Toutes ces substances sont des médiateurs de la douleur induite aussi bien par l’inflammation que par les lésions du système nerveux.
L’activation gliale est liée significativement au développement des douleurs. Les cellules microgliales activées via l’expression de certains récepteurs comme le toll-like 2 (TLR2) ou le récepteur ionotropique aux purines (le P2X4), dont leurs expressions semblent conduire à une hyperexcitabilité des neurones spinaux. L’activation des récepteurs P2X4 entraîne ainsi une libération accrue de BDNF par la microglie, qui serait la responsable des interactions glie-neurones conduisant à l’hyperexcitabilité de ces derniers. L’action du BDNF changerait le potentiel d’équilibre anionique et inverserait ainsi l’effet de l’ouverture des canaux chlore par la glycine et l’acide gamma amino butyrique (GABA) [17,20,21].
L’inhibition de l’activité métabolique de la microglie, le blocage de son activation ou des produits qu’elle secrète (le BDNF), l’administration de cytokines anti-inflammatoires (interleukine-10 par exemple) réduisent l’hyperalgésie et l’allodynie dans les modèles animaux [11,22,23]]. Les chémokines qui sont des cytokines dont le rôle principal est l’activation cellulaire et la stimulation de la migration des leucocytes, interviendraient aussi dans la douleur neuropathique. Ainsi certains récepteurs aux chémokines tels les CCR2, CCR5 (qui interagit avec le récepteur opioïde μ), CXCR4, le CX3CR1 situés au niveau de la corne dorsale de la moelle peuvent potentiellement altérer le message algique. Leur modulation régulerait les interactions neuro-gliales en agissant sur l’activité de récepteurs de NMDA dans les neurones de la corne dorsale [17,18,22].
Mécanismes d’action de l’acupuncture et de l’électroacupuncture (EA) dans la douleur neuropathique
Depuis quelques années, de nombreuses recherches ont porté sur les mécanismes d’action de l’électroacupuncture et de l’acupuncture essentiellement dans la douleur neuropathique. Différents modèles expérimentaux d’animaux ont été utilisés pour comprendre son effet analgésique chez les rats. On a pu ainsi mettre en évidence des effets sur les opioïdes endogènes au niveau de la corne postérieure de la moelle, les effets adrénergiques et sérotoninergiques, cholinergiques et GABAergiques, sans oublier les effets locaux et sur la microglie.
Il existe plusieurs niveaux de modulation de la douleur : périphérique, segmentaire et supra-spinal (figure 3).
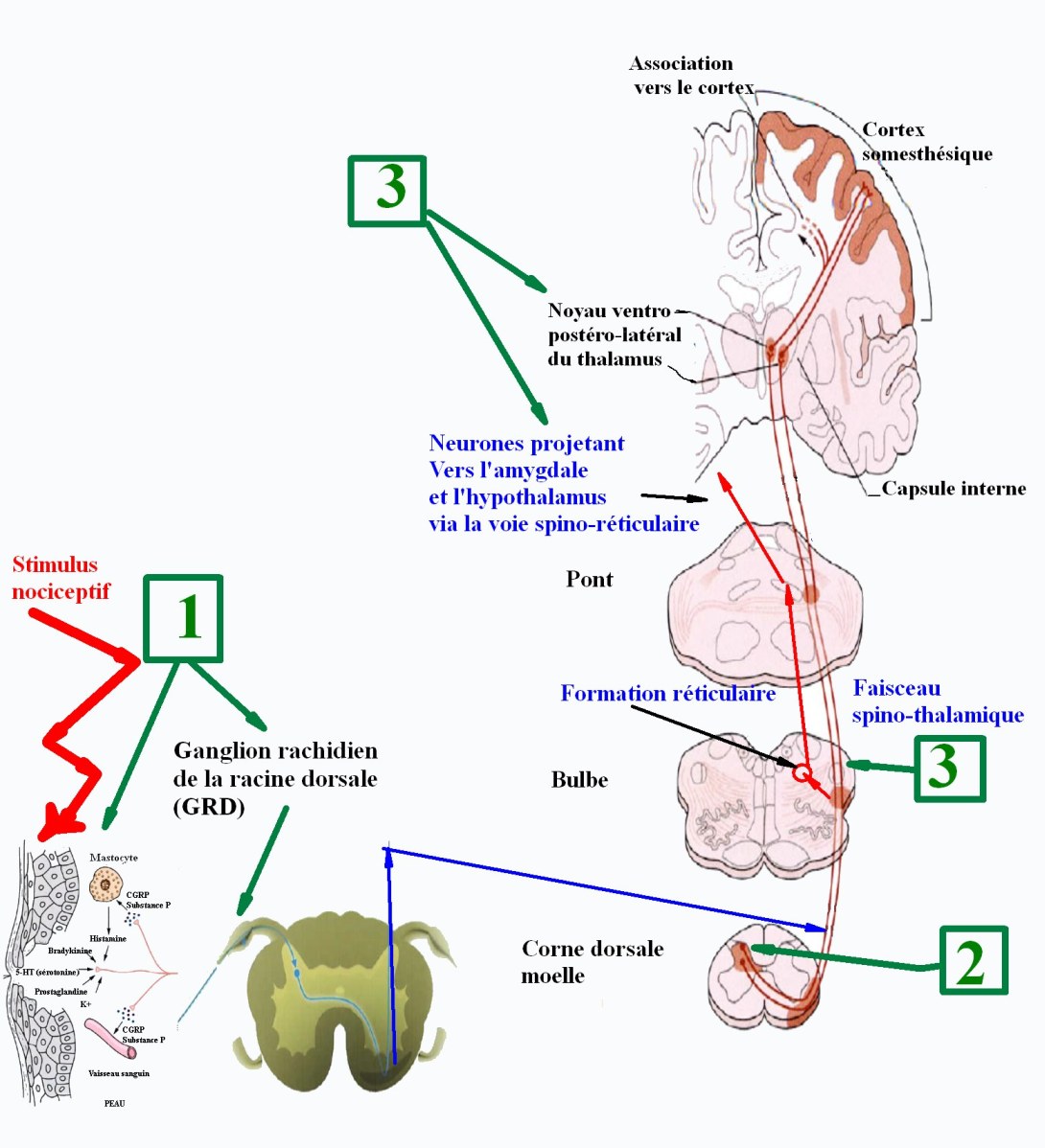
Figure 3. Plusieurs niveaux de modulation : 1. Périphérique avec action sur la transduction au niveau des cellules du derme et du ganglion rachidien de la racine dorsale (GRD) ; 2. Segmentaire au niveau de la corne postérieure, théorie du portillon ; 3. Supra-spinal : modulation du tronc cérébral, hypothalamus, thalamus, formation réticulaire, du bulbe etc. Vont intervenir les différents opioïdes et leurs récepteurs, les récepteurs adrénergiques, cholinergiques, sérotoninergiques, GABAergiques, au glutamate. La modulation de la douleur s’effectuera via l’action sur la sensibilisation périphérique, centrale, la substance gliale, les cytokines.
Action de l’acupuncture sur la sensibilisation périphérique
Adénosine
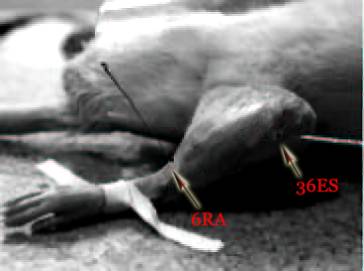
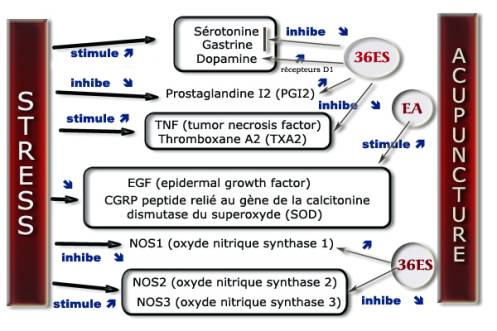
L’ATP est libérée en réponse à une stimulation thermique, mécanique voire électrique. Une fois libérée, l’ATP agit comme un transmetteur qui se lie aux récepteurs purinergiques de type P2X et P2Y. L’ATP ne peut pas être transportée dans la cellule mais se dégrade rapidement en adénosine avant la réabsorption. Or l’adénosine en se fixant au récepteur à l’adénosine A1 va avoir une action analgésique dans les douleurs chroniques (allodynie mécanique ou thermique) de type neuropathique (par ligature du nerf sciatique) ou inflammatoire (injection de l’adjuvant complet de Freund) créé sur un modèle de souris. Goldman et coll. l’ont démontré en puncturant le 36ES avec recherche du deqi. Le taux d’adénosine dans les tissus était vingt-quatre fois supérieur au taux avant traitement. L’acupuncture a permis de soulager les souris à l’exception des souris chez lesquelles les récepteurs à l’adénosine étaient désactivés (par exemple des animaux ayant subi des mutations sur les récepteurs en question), ce qui confirme le rôle de la molécule dans le processus antidouleur (figure 4) [[24]].
Une autre étude montre qu’en plus de l’adénosine, l’acupuncture entraînerait une libération d’autres agonistes puriniques (ATP, ADP, UTP…). En se liant aux récepteurs puriniques (P2yR2, P2yR4, P2yR1 et P2xR7) sur les fibroblastes à proximité, le Ca2+ cytosolique est augmenté engendrant un remodelage du cytosquelette d’actine. Les changements de cytosquelette d’actine surviennent lentement et culminent 10 min après l’exposition à l’agoniste et pourraient intervenir également dans l’action antalgique de l’acupuncture [[25]].
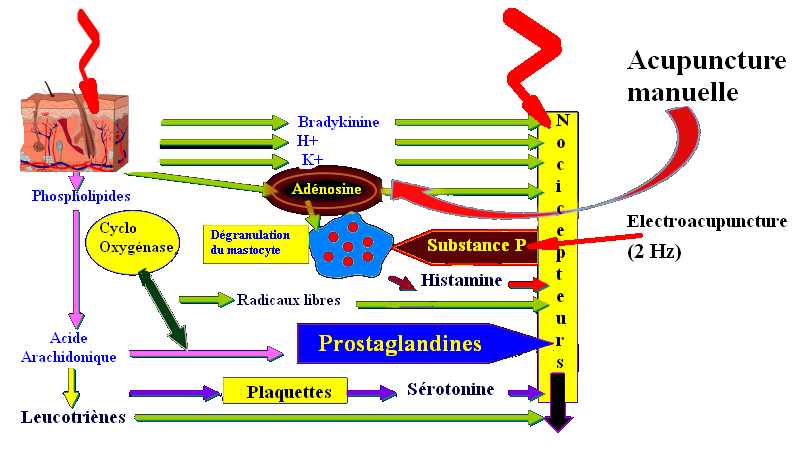
Figure 4. Action de l’acupuncture et de l’EA (2 Hz) sur les sensibilisations périphérique et centrale.
Récepteurs vanilloïdes (VR1 ou TRPV1)
Les récepteurs vanilloïdes sont des récepteurs-canaux cationiques qui, à l’état ouvert, laissent entrer dans la cellule le calcium et le sodium, ce qui crée une dépolarisation. Les VR1 sont localisés à la surface des nerfs sensitifs périphériques au niveau de la surface cutanée, les muqueuses, certaines régions du SNC et de la moelle épinière… Les récepteurs TRPV sont activés par des stimuli mécaniques, thermiques (chaud et froid), par l’acidité et certaines substances chimiques comme la capsaïcine. Ce produit naturel trouvé dans le piment rouge a une action biphasique ; elle stimule au premier contact les récepteurs VR1 provoquant une douleur et ensuite par contact prolongé inhibe, désensibilise les récepteurs entraînant un effet analgésique.
Ainsi le récepteur vanilloïde 1 (TRPV1) joue un rôle clé dans la douleur neuropathique. Jiang et coll., sur un modèle animal de douleur neuropathique par ligature de la racine rachidienne L5 droite chez le rat, ont montré que la stimulation d’EA (2Hz, 2mA, 0,4ms) inhibe le TRPV1 au niveau du ganglion de la racine dorsale (DRG) L5 en réduisant l’allodynie mécanique dans la patte postérieure du rat ipsilatérale. Par ailleurs, le calcitonin gene-related peptide (CGRP) est également inhibé de la même manière que le TRPV1 [[27]].
Action de l’acupuncture sur la sensibilisation centrale et la potentialisation à long terme
Substance P et β-endorphine
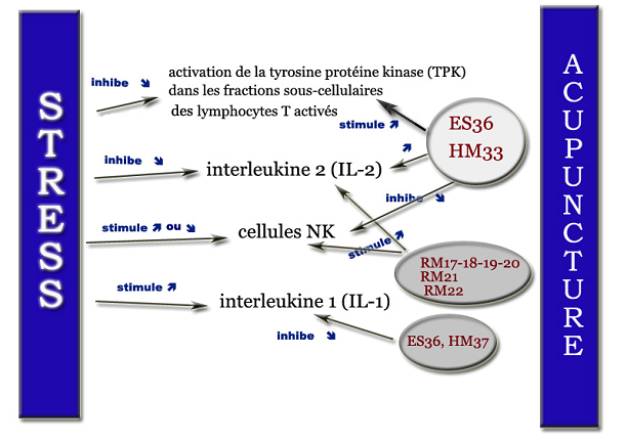
Sur un modèle expérimental (souris) de douleur neuropathique liée à une inoculation de cellules cancéreuses de sarcome au voisinage du nerf sciatique avec allodynie et hyperalgie, l’EA à 2Hz (durée d’impulsion 0,25ms) est appliquée sur le point zusanli (ES36). Lee et coll. observe une réduction de la douleur qui s’accompagne d’une diminution de la substance P au niveau de la corne postérieure de la moelle et une augmentation de la concentration de β-endorphines dans le sang et le cerveau [[26]] (figure 4).
Après ligature des racines L5 et L6 sur un modèle animal de rat, la sensibilisation centrale, la potentialisation à long terme (LTP) et la plasticité synaptique au niveau de la corne dorsale de la moelle contribuent au développement et à l’entretien des douleurs neuropathiques. L’étude de Xing et coll a étudié les changements de plasticité synaptique médullaire et sa modulation par EA. A basse fréquence, l’EA (2 Hz) appliquée sur les points d’acupuncture ES36 et RA6 va induire une dépression à long terme (LTD) des potentiels évoqués des fibres C et améliorer de ce fait la douleur neuropathique. Cet effet est bloqué par l’antagoniste MK-801 des récepteurs glutamiques de l’acide N-méthyl-D-aspartique (NMDA) et par la naloxone, antagoniste des récepteurs opioïdes. En revanche, l’EA à haute fréquence (100 Hz) n’est pas efficace dans le traitement des douleurs neuropathiques et induit au contraire une LTP sur le modèle de rat neuropathique alors qu’on observe une LTD dans le groupe de rats opérés de manière fictive (car tributaire du système GABAergic endogène et du système d’inhibition sérotoninergique. En bref, l’EA à basse ou haute fréquence a un effet différent sur la modulation de la plasticité synaptique de la moelle chez le rat avec douleur neuropathique. La modulation différente de la moelle en LTD ou LTP par l’EA basse ou haute fréquence est un mécanisme potentiel de différents effets analgésiques de l’EA dans la douleur neuropathique. L’EA à 2Hz contribue essentiellement aux effets analgésiques de longue durée [[28]] (figure 5).
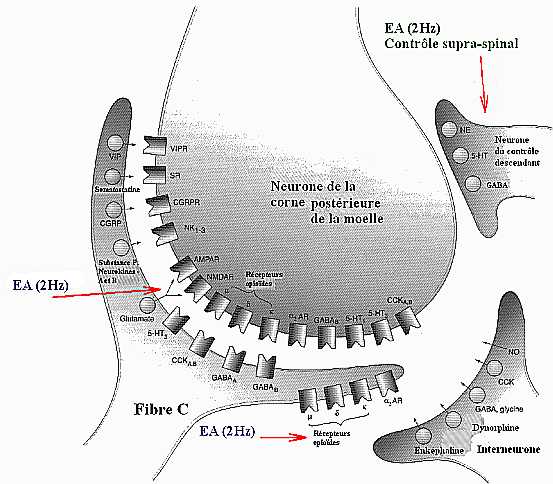
Figure 5. Sensibilisation centrale. Action de l’EA à 2Hz sur les différents récepteurs et neuromédiateurs au niveau de la corne postérieur de la moelle.
Inhibition de l’activité métabolique de la microglie
Les cellules gliales de la moelle épinière (microglie et astrocytes) contribuent au développement et à l’entretien de la douleur inflammatoire mais aussi neuropathique [[29]]. Ainsi l’activation de la microglie, des astrocytes et la libération des cytokines pro-inflammatoires vont jouer un rôle dans l’induction d’un état d’hypersensibilité de type hyperalgésie et allodynie [[30]].
Shan et coll. ont ainsi démontré sur un modèle animal de douleur inflammatoire (injection de CFA dans la cheville de rat) que l’EA (2 Hz/100Hz en alternance) aux points ipsilatéraux huantiao (30VB) et yanglingquan (34VB) a significativement réduit l’hypersensibilité (allodynie et hyperalgésie) nociceptive et l’activation de la microglie au niveau médullaire en réduisant la régulation positive (up-regulation) de l’IL-1β, IL-6 et les niveaux d’ARNm de TNF-α [[31]].
De même, l’EA (2/60Hz en alternance) sur un modèle animal de stress chirurgical va supprimer l’expression des cytokines pro-inflammatoires à la fois au niveau plasmatique et splénique, régulation indépendante des surrénales et de la corticostérone. L’EA va réguler de façon négative (« down-regulation »), non seulement l’expression des récepteurs toll-like 2 et 4 (TLR2/4), mais va aussi inhiber la production et la sécrétion de cytokines pro-inflammatoires (IL-1β, IL-6 et TNF-α) au niveau de la rate [[32]].
Gim et coll vont également objectiver que l’EA à basse fréquence (2Hz, 0,5ms) sur un modèle expérimental de douleurs neuropathiques (section des racines nerveuse S1 et S2 chez le rat) va atténuer l’allodynie à la chaleur. Les auteurs montrent que l’EA supprime l’activation de la microglie et des astrocytes en inhibant la libération de cytokines pro-inflammatoires comme le TNF-α, IL-6, IL-1β, mais va aussi supprimer l’activation au niveau de la corne postérieure des métalloprotéases matricielles MMP-9 et MMP-2 qui sont impliquées dans la neuro-inflammation [[33]].
De même, sur un modèle expérimental de maladie de Parkinson chez le rat, l’étude de Kang et coll. suggère l’action neuroprotectrice et anti-inflammatoire de l’acupuncture manuelle (aiguilles placées au FO3 et VB34 et tournées deux fois par seconde durant 15 s) par inhibition de l’activation microgliale. L’acupuncture contribue à atténuer l’augmentation du macrophage antigen complex-1 (MAC-1), marqueur de l’activation microgliale, et réduit l’augmentation de la cyclooxygénase-2 (COX2) et celle de l’expression de la forme inductible (iNOS ou NOS2) de l’oxyde nitrique dans le striatum et la substantia nigra [[34]].
Une autre étude sur un modèle animal (rat) de douleur neuropathique par laminectomie au niveau des racines dorsales D9-D10 s’est intéressée à l’effet antalgique de l’acupuncture manuelle. L’acupuncture manuelle (stimulation par rotation deux cycles par seconde pendant 30s et laissées en place durant 30mn des points shuigou(VG26) et yanglingquan), soulage l’allodynie mécanique et l’hyperalgésie thermique. On constate également la diminution de l’activation de la microglie par inhibition de la signalisation des MAP kinases (Mitogen-activated protein) impliquant la MAP kinase p38 et ERK (Extracellular signal-regulated kinase). De ce fait, il y a aussi une diminution du taux de prostaglandine E2 (PGE2), produite via la signalisation ERK et les récepteurs PGE2 et qui est médiatrice de la douleur. En outre, Choi et coll. ont constaté que l’acupuncture inhibe aussi la production de dérivés réactifs de l’oxygène (reactive oxygen species, ROS) comme l’anion superoxyde (O2-) qui agit comme un modulateur de l’activation de la microglie [[35]].
A noter que cette action analgésique de l’acupuncture sur la modulation de la signalisation des MAP kinases s’observera également avec EA (2/15Hz) sur un modèle de douleur neuropathique (ligature du nerf sciatique) un niveau de l’hippocampe [[36]]. La figure 6 récapitule l’action de l’acupuncture et de l’EA à 2Hz
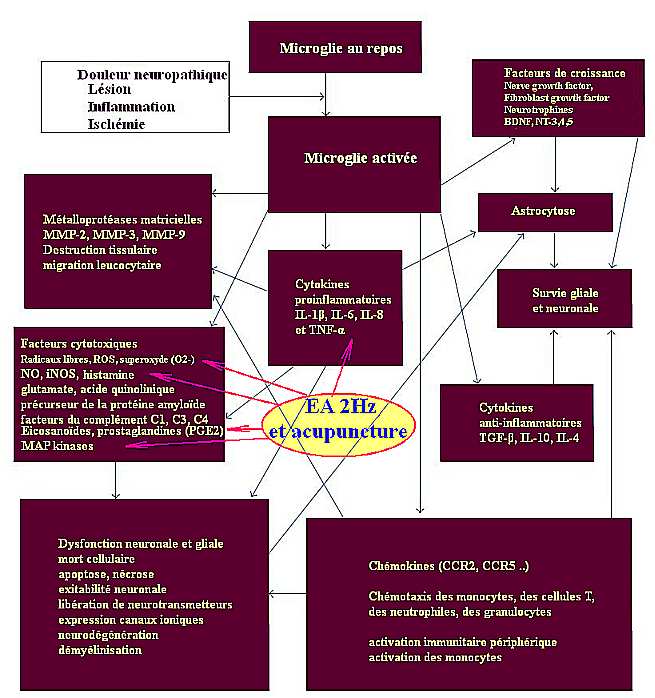
Figure 6. Action de l’acupuncture et de l’EA à 2 Hz dans la modulation des mécanismes neuro-inflammatoires au niveau de la microglie.
Conclusion
Après avoir vu la biologie au niveau de la sensibilisation périphérique et centrale, nous verrons dans un prochain article la modulation de la douleur neuropathique par l’acupuncture ou l’EA via l’activation des différents mécanismes inhibiteurs descendants. Ainsi dans la douleur de type nociceptive, il semble que l’intensité de l’effet antalgique de l’EA à 2 Hz repose sur des mécanismes descendants noradrénergiques et implique des mécanismes opioïdes et muscariniques de la corne postérieure de la moelle. La durée de l’effet de l’EA à 2 Hz dépend par contre à la fois de mécanismes noradrénergiques et sérotoninergiques descendants et implique la modulation GABAergique de la corne postérieure. En revanche, l’intensité de l’EA à 100 Hz agirait par des mécanismes spinaux muscariniques, opioïdes, et GABAergiqueB, tandis que la durée des effets dépendrait de mécanismes sérotoninergiques, muscariniques, opioïdes et GABAergiqueA [[37]].
Références
[1]. Référentiels interrégionaux (RIR) en soins oncologiques de support. Neuropathie périphérique et cancer. Référentiel 2012. AFSOS. Available from: URL http://www.afsos.org/IMG/pdf/Neuropathie_peri-2.pdf.
[2]. Grisold W, Cavaletti G, Windebank AJ. Peripheral neuropathies from chemotherapeutics and targeted agents: diagnosis, treatment, and prevention. Neuro Oncol. 2012;14 Suppl 4:iv45-54.
[3]. Argyriou AA, Bruna J, Marmiroli P, Cavaletti G. Chemotherapy-induced peripheral neurotoxicity (CIPN): an update. Crit Rev Oncol Hematol. 2012;82(1):51-77.
[4]. Lebrun C, Frenay M. [Neurologic side effects of cytotoxic drugs]. Rev Med Interne. 2010;31(4):295-304.
[5]. Saïd G. [Progressive centripetal degeneration in polyneuropathies]. Rev Neurol (Paris). 1981;137(10):573-88.
[6]. Windebank AJ, Grisold W. Chemotherapy-induced neuropathy. J Peripher Nerv Syst. 2008;13(1):27-46.
[7]. Lebrun C, Frenay M. Neurotoxicité des chimiothérapies chez l’adulte. Rev Neur (Paris). 2003;159(8-9):741-754.
[8]. LaPointe NE, Morfini G, Brady ST, Feinstein SC, Wilson L, Jordan MA. Effects of eribulin, vincristine, paclitaxel and ixabepilone on fast axonal transport and kinesin-1 driven microtubule gliding: implications for chemotherapy-induced peripheral neuropathy. Neurotoxicology. 2013;37:231-9.
[9]. Calvino B, Thibault K. Apport des modèles expérimentaux dans la compréhension des douleurs en cancérologie. Douleurs Evaluation-Diagnostic –Traitement. 2010;11:26-36.
[10]. Scholz J, Woolf CJ. The neuropathic pain triad: neurons, immune cells and glia. Nat Neurosci. 2007;10(11):1361-8.
[11]. Le Bars D, Willer JC. Physiologie de la douleur. EMC – Anesthésie-Réanimation. 2004;1(4):227-266.
[12]. Chauvin M. Physiologie et pharmacologie de la douleur. In: Les Essentiels. Ed Elsevier Masson SAS; 2006.p. 323-334.
[13]. Nakamura M, Jang IS. Presynaptic nicotinic acetylcholine receptors enhance GABAergic synaptic transmission in rat periaqueductal gray neurons. Eur J Pharmacol. 2010 Aug 25;640(1-3):178-84.
[14]. Umana IC, Daniele CA, McGehee DS. Neuronal nicotinic receptors as analgesic targets: It’s a winding road. Biochem Pharmacol. 2013;86(8):1208-14.
[15]. Park CH, Lee HG, Lee SH, Chung CW, Yoon MH. The role of adrenergic and cholinergic receptors on the antinociception of sildenafil in the spinal cord of rats. Neurosci Lett. 2011;502(2):99-102.
[16]. Cai YQ, Chen SR, Han HD, Sood AK, Lopez-Berestein G, Pan HL. Role of M2, M3, and M4 muscarinic receptor subtypes in the spinal cholinergic control of nociception revealed using siRNA in rats. J Neurochem. 2009;111(4):1000-10.
[17]. Ramesh G, MacLean AG, Philipp MT. Cytokines and chemokines at the crossroads of neuroinflammation, neurodegeneration, and neuropathic pain. Mediators Inflamm. 2013;2013:480739. doi: 10.1155/2013/480739.
[18]. Zhuo M, Wu G, Wu LJ. Neuronal and microglial mechanisms of neuropathic pain. Mol Brain. 2011;4:31.
[19]. Zhuo M. Neuronal mechanism for neuropathic pain. Mol Pain. 2007 Jun 6;3:14.
[20]. Kim D, Kim MA, Cho IH, Kim MS, Lee S, Jo EK, Choi SY, Park K, Kim JS, Akira S, Na HS, Oh SB, Lee SJ. A critical role of toll-like receptor 2 in nerve injury-induced spinal cord glial cell activation and pain hypersensitivity. J Biol Chem. 2007 May 18;282(20):14975-83.
[21]. Shi XQ, Zekki H, Zhang J. The role of TLR2 in nerve injury-induced neuropathic pain is essentially mediated through macrophages in peripheral inflammatory response. Glia. 2011 Feb;59(2):231-41.
[22]. Gao YJ, Ji RR. Chemokines, neuronal-glial interactions, and central processing of neuropathic pain. Pharmacol Ther. 2010 Apr;126(1):56-68.
[23]. Garcia-Larrea L, Magnin M. [Pathophysiology of neuropathic pain: review of experimental models and proposed mechanisms]. Presse Med. 2008 Feb;37(2 Pt 2):315-40.
[24]. Goldman N, Chen M, Fujita T, Xu Q, Peng W, Liu W, Jensen TK, Pei Y, Wang F, Han X, Chen JF, Schnermann J, Takano T, Bekar L, Tieu K, Nedergaard M. Adenosine A1 receptors mediate local anti-nociceptive effects of acupuncture. Nat Neurosci. 2010 Jul;13(7):883-8.
[25]. Goldman N, Chandler-Militello D, Langevin HM, Nedergaard M, Takano T. Purine receptor mediated actin cytoskeleton remodeling of human fibroblasts. Cell Calcium. 2013 Apr;53(4):297-301.
[26]. Lee HJ, Lee JH, Lee EO, Lee HJ, Kim KH, Lee KS, Lee CH, Nam DW, Kim SH, Lee HJ, Ahn KS. Substance P and beta endorphin mediate electroacupuncture induced analgesic activity in mouse cancer pain model. Acupunct Electrother Res. 2009;34(1-2):27-40.
[27]. Jiang YL, Yin XH, Shen YF, He XF, Fang JQ. Low Frequency Electroacupuncture Alleviated Spinal Nerve Ligation Induced Mechanical Allodynia by Inhibiting TRPV1 Upregulation in Ipsilateral Undamaged Dorsal Root Ganglia in Rats. Evid Based Complement Alternat Med. 2013;2013:170910.
[28]. Xing GG, Liu FY, Qu XX, Han JS, Wan Y. Long-term synaptic plasticity in the spinal dorsal horn and its modulation by electroacupuncture in rats with neuropathic pain. Exp Neurol. 2007 Dec;208(2):323-32.
[29]. Watkins LR, Hutchinson MR, Johnston IN, Maier SF. Glia: novel counter-regulators of opioid analgesia. Trends Neurosci. 2005 Dec;28(12):661-9.
[30]. Raghavendra V, Tanga F, DeLeo JA. Inhibition of microglial activation attenuates the development but not existing hypersensitivity in a rat model of neuropathy. J Pharmacol Exp Ther. 2003;306(2):624-30.
[31]. Shan S, Qi-Liang MY, Hong C, Tingting L, Mei H, Haili P, Yan-Qing W, Zhi-Qi Z, Yu-Qiu Z. Is functional state of spinal microglia involved in the anti-allodynic and anti-hyperalgesic effects of electroacupuncture in rat model of monoarthritis? Neurobiol Dis. 2007;26(3):558-68.
[32]. Wang J, Zhao H, Mao-Ying QL, Cao XD, Wang YQ, Wu GC. Electroacupuncture downregulates TLR2/4 and pro-inflammatory cytokine expression after surgical trauma stress without adrenal glands involvement. Brain Res Bull. 2009;80(1-2):89-94.
[33]. Gim GT, Lee JH, Park E, Sung YH, Kim CJ, Hwang WW, Chu JP, Min BI. Electroacupuncture attenuates mechanical and warm allodynia through suppression of spinal glial activation in a rat model of neuropathic pain. Brain Res Bull. 2011;86(5-6):403-11.
[34]. Kang JM, Park HJ, Choi YG, Choe IH, Park JH, Kim YS, Lim S. Acupuncture inhibits microglial activation and inflammatory events in the MPTP-induced mouse model. Brain Res. 2007 Feb 2;1131(1):211-9.
[35]. Choi DC, Lee JY, Lim EJ, Baik HH, Oh TH, Yune TY. Inhibition of ROS-induced p38MAPK and ERK activation in microglia by acupuncture relieves neuropathic pain after spinal cord injury in rats. Exp Neurol. 2012;236(2):268-82.
[36]. Gao YH, Chen SP, Wang JY, Qiao LN, Meng FY, Xu QL, Liu JL. Differential proteomics analysis of the analgesic effect of electroacupuncture intervention in the hippocampus following neuropathic pain in rats. BMC Complement Altern Med. 2012 Dec 2;12:241.
[37]. Silva JR, Silva ML, Prado WA. Analgesia induced by 2- or 100-Hz electroacupuncture in the rat tail-flick test depends on the activation of different descending pain inhibitory mechanisms. J Pain. 2011;12(1):51-60.