Résumé : La transduction est l’une des clefs du mécanisme d’action de l’acupuncture. Elle permet par l’intermédiaire de récepteurs transmembranaires (récepteurs tyrosine-kinases, récepteurs couplés aux protéines G, récepteurs à cytokines etc..) d’engendrer les protéines cibles. Cette étude explore au travers de l’acupuncture expérimentale la complexité de la signalisation cellulaire activée grâce aux récepteurs de la membrane plasmique. Bases de la signalisation autocrine, paracrine, synaptique, voire hormonale, les molécules informationnelles sont très nombreuses : TNF-a, IL2, interférons, TGF, NGFR, PDGF, VEGF, TEK, IGF1, EGFR etc.. Cette revue bibliographique met en exergue les principales activées par l’acupuncture. Mots-clés : transduction – mécanisme de l’acupuncture – récepteurs tyrosine-kinase – cytokine – revue.
Summary: Transduction is one of the keys of the mechanism of action of acupuncture. It allows via transmembrane receptors (receptor tyrosin-kinases, receptor coupled with the proteins G, cytokine receptors etc.) to activate target proteins. This study explores through experimental acupuncture the complexity of the cellular pathways activated thanks to the receptors of the plasmic membrane. Bases of autocrine, paracrine, synaptic, even hormonal pathways, the informational molecules are very numerous: TNF-a, IL2, let us interfere, TGF, NGFR, PDGF, VEGF, TEK, IGF1, EGFR etc. This bibliographical review puts forward the principal ones activated by acupuncture. Keywords: transduction – mechanism of acupuncture – receptors tyrosin-kinase – cytokine – review.
Après avoir vu dans un précédent article [ [1] ] les mécanismes de la mécanotransduction, nous allons continuer l’exploration du mode d’action de l’acupuncture en étudiant la transduction. On sait par exemple que l’augmentation de l’expression de l’ARNm de la cyclooxygenase 2 (cox2) en réponse à un stress est bloquée par la cytochalasine D. Celle-ci est inhibitrice aussi des microfilaments d’actine du cytosquelette que l’on sait très impliqués dans la mécanotransduction liée à la puncture de l’aiguille, montrant ainsi l’intervention de l’actine dans la synthèse de cox2 [ [2] ]. On sait aussi que la cox2 est une enzyme intervenant dans la transduction des prostaglandines par l’intermédiaire du récepteur prostaglandine F (PTGFR) couplé à la protéine G. La transduction peut faire ainsi suite à la mécanotransduction, être en relation avec une activation par voie auto, paracrine, synaptique, hormonale voire entrer dans le cadre de la neuromodulation. Par une analyse protéomique des différentes protéines exprimées lors de douleurs neuropathiques sur un modèle de rat Sprague-Dawley, Sung et coll. ont détecté trente-six protéines.

L’action de l’électroacupuncture (EA) appliquée au zusanli (ES36) restaurent l’expression normale des protéines. Sung et coll. constatent que vingt et une de ces protéines identifiées sont impliquées dans un certain nombre de processus biologiques dont l’inflammation, le métabolisme enzymatique et les signaux de transduction [ [3] ]. De la même manière en 2006, Zhou et coll. ont montré l’intervention des signaux cellulaires de transduction lors du traitement acupunctural par le méridien de Coeur lors d’une ischémie myocardiaque expérimentale [ [4] ]. Le message moléculaire (hormones, neurotransmetteurs, facteurs trophiques) permet d’assurer les grandes fonctions physiologiques et doit être détecté par les cellules cibles sur lesquelles il agit. Cela correspond au message délivré par la transduction en rapport avec l’activation des protéines transmembranaires ou récepteurs sensibles aux molécules présentes dans le milieu extracellulaire ou sensibles aux facteurs physiques. L’interaction spécifique entre une molécule intercellulaire et un de ses récepteurs entraîne des réactions en cascade à partir de la face intracellulaire de la membrane plasmique : c’est le processus de transduction du signal. Au terme, par la synthèse de molécules informationnelles protéines cibles, le signal pourra être autocrine, paracrine, synaptique voire hormonal. Cette étude fait la revue des mécanismes de la transduction impliquant les récepteurs transmembranaires à tyrosine-kinases, à cytokines et une cascade de molécules informationnelles lors de l’action de l’acupuncture.
Signalisation cellulaire
La signalisation cellulaire se fait par deux voies différentes.
A proximité de la cellule
Signalisation paracrine
Les cellules émettrices et les cellules cibles sont des types cellulaires différentes. Les cellules émettrices produisent et délivrent un signal vers les cellules cibles situées à proximité.
Signalisation autocrine
Les cellules émettrices et les cellules cibles sont de même type cellulaire. Les cellules produisent un signal qui peut se fixer sur ses propres récepteurs. Ce type de transmission permet de coordonner l’action d’un groupe cellulaire
A distance de la cellule
Deux types de cellules, les neurones et les cellules endocriniennes interviennent dans cette signalisation à distance qui seront respectivement la signalisation synaptique et la signalisation hormonale. En effet, les neurones par l’intermédiaires de leurs axones entrent en contact avec des cellules cibles éloignées, avec envoi d’un potentiel d’action et libération de neurotransmetteurs dans la fente synaptique, tandis que les cellules endocrines libèrent directement leurs molécules informationnelles dans le sang et transmettent donc leur signal à des distances énormes à l’échelle cellulaire (figure 1).
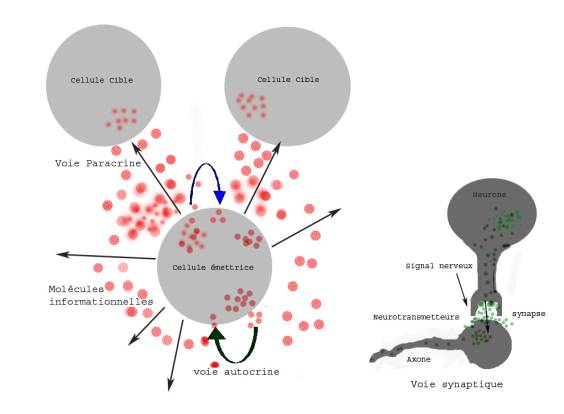
Figure 1. Les signalisations autocrine, paracrine et synaptique.
Les récepteurs impliqués dans la transduction cellulaire
Un système transductionnel transforme un type de signal biochimique en un autre type de signal biochimique (par exemple une activité enzymatique intracellulaire ou nucléaire). La transduction fait intervenir plusieurs types de récepteurs : les récepteurs métabotropiques (les récepteurs à activité tyrosine-kinase, les protéines G, les récepteurs guanylyl-cyclases, les récepteurs ionotropiques (les canaux ioniques calciques, potassiques, sodiques, les récepteurs à neurotransmetteurs comme les récepteurs NMDA, GABA, nicotinique, AMPA, 5HT3 etc..), les récepteurs à cytokine etc.. Des enzymes comme la famille des NAD(P)H oxydases (NOX1, NOX2 etc.) entraînant une libération de radicaux libres oxygénés (superoxyde O–2) interagissant avec le monoxyde d’azote interviennent aussi dans les mécanismes de la transduction cellulaire. Il existe à l’heure actuelle environ 87 récepteurs à activité tyrosine-kinase, regroupés selon leur organisation structurale en plusieurs familles. L’activation d’un ou plusieurs de ces récepteurs peut conduire à l’entrée du calcium ou à l’activation de différentes cascades biochimiques par les protéines effectrices qui sont soit des enzymes (AMP cyclique, GMP cyclique, phospholipase C ou A2), soit des canaux ioniques ou des transporteurs de neurotransmetteurs. En effet, dans une même cellule les systèmes de transduction peuvent interagir les uns avec les autres. Plusieurs systèmes de transduction peuvent être activés simultanément et même interférer entre eux pour générer une réponse physiologique complexe.
Le signal intracellulaire métabotrophique revêt souvent deux formes : réaction de phosphorylation par addition d’atomes de phosphore sur des protéines ou synthèse de molécules de signalisation intracellulaire, les seconds messagers. Cette dualité résulte essentiellement de l’existence de deux sous-groupes de récepteurs : les récepteurs tyrosine-kinases (phosphorylation) et les récepteurs couplés aux protéines G (activation des seconds messagers). En général, les molécules informationnelles extracellulaires activent les signaux de transduction par leurs actions sur des récepteurs métabotropiques couplés à des protéines G lorsqu’il s’agit de neurotransmetteurs et sur des récepteurs tyrosine-kinases lorsqu’il s’agit de mitogènes (neurotrophines et autres facteurs de croissance).
L’action d’un récepteur métabotropique est plus lente que celle d’un récepteur ionotropique (ce sont aussi des récepteurs pour neurotransmetteurs qui agissent en quelques millièmes de secondes) en raison des réactions enzymatiques en cascade nécessaires à la genèse des seconds messagers et de l’action des seconds messagers sur les protéines présentes dans la cellule. Ainsi la latence d’une réponse cellulaire finale initiée via un récepteur métabotropique se chiffre en minute, voire heure [ [5] ].
Les récepteurs tyrosine-kinases
Comme les intégrines impliquées essentiellement dans le mécanisme de mécanotransduction, ces récepteurs possèdent une activité enzymatique de phosphorylation dont les cibles sont les résidus tyrosines des protéines. Les principaux récepteurs tyrosines-kinases sont : platelet-derived growth factor (PDGF), vascular endothelial growth factor (VEGF), TEK tyrosine kinase (TEK), epidermal growth factor (EGF), fibroblast growth factor (FGF), insulin-like growth factor 1 (IGF1), anaplastic lymphoma kinase (ALK), neurotrophic tyrosine receptor kinase (NTRK2) (voir figure 2).
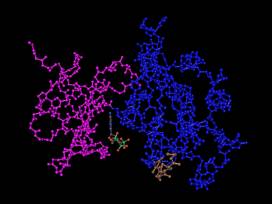 |  | 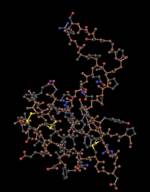 |
Figure 2. Les structures du récepteurs IGF1, du domaine catalytique de la tyrosine kinase (TyrKc) et de l’IGF1.
Une activité de kinase s’enclenche lorsque le médiateur se fixe sur le récepteur tyrosine-kinase. Il y a alors apparition de tyrosines phosphorylées qui vont entraîner soit l’activation en chaîne d’une cascade de kinases, soit l’activation de protéines dites « adaptateurs » (Shc, Grb2, GEF, flk1, Sos&) :
– l’activation en chaîne d’une cascade de kinases par phosphorylation va stimuler la phophatidylinositol-3-kinase (PI3K), puis la protéine AKT ; une autre cascade de réactions passe par la phosphorylation de la phospholipase C (PLC) et comme pour les protéines G, activation de la calmoduline kinase (CaMK) par la voie de l’IP3 (inositol triphosphate) et par la voie de la diacylglycérol (DAG), activation de la kinase C (PKC), puis du mitogen-activated protein kinase kinase (MEK), du mitogen activated protein kinase (MAPK) et enfin de l’ERK (extracellularly regulated kinase).
– les protéines dites « adapteurs » stimulent une protéine G particulière : la protéine Ras dont le rôle est d’activer des kinases (les MAP kinases et les protéines kinases). L’essentiel du mécanisme de transduction repose, comme dans la mécanotransduction, sur la cascade de réactions de phosphorylation déclenchant une modification du fonctionnement cellulaire avec transcription et biosynthèse de protéines cibles.
Action de l’acupuncture sur les facteurs de transcription avec modifications de l’expression génique
Chez le macaque rhésus, une technique à micromatrice d’ADN a été employée pour analyser le profil de l’expression génétique dans l’ischémie résultante d’une occlusion d’une artère cérébrale et lors d’une ischémie traitée par électroacupuncture. Il s’avère que dans le groupe EA – ischémie, 10% du total des gènes examinés (8% de gènes dans le groupe ischémie seul) ont été affectés, et ceci en rapport avec des gènes liés à un signal de transduction, une réponse au stress, des gènes de réparation de l’ADN. Un des plus représentatifs de ces gènes est l’expression de l’ARNm de l’insuline-like growth factor-1 (IGF1) dans le striatum et l’hippocampe [ [6] ].
Une atteinte de la muqueuse gastrique stress induite par immersion dans l’eau et immobilisation a été traitée par électroacupuncture par les points du méridien d’Estomac (sibai : ES2, liangmen : ES21, zusanli : ES36 ; groupe ES : n = 12), par les points du méridien de Vésicule Biliaire ( yangbai : 14VB, riyue : 24VB, yanglingquan : 34VB ; groupe VB : n = 12), le tout randomisé avec trois autres groupes (groupe normal n = 8 ; groupe modèle n = 8 ; groupe sérum n = 12). Yang et coll. observent que l’expression du gène du récepteur de l’epidermal growth factor receptor (ARNm EGFR) est plus élevée de manière statistiquement significative (p<0,01) dans le groupe ES par rapport aux autres groupes [ [7] ].
Une autre étude a objectivé que l’électroacupuncture appliquée sur le ES36 (zusanli) influence l’expression de la brain-derived neurotrophic factor (BDNF) dans l’hippocampe d’un groupe de rats exposés à un stress d’immobilisation dans des saCoe en plastique. L’analyse de la réaction de polymérase et l’isolation de la transcription de l’ARN montrait que la stimulation électroacupuncturale restaurait de manière statistiquement significative l’expression de l’ARNm du BDNF chez les rats soumis à un stress d’immobilisation [ [8] ]. Le BDNF est la protéine encodée par le gène de la cytokine nerve growth factor (NGFR) et peut être aussi le ligand d’un récepteur tyrosine kinase, le tropomyosin receptor kinase B (TrkB).
Action de l’acupuncture sur les facteurs trophiques
Les récepteurs NMDA (composés d’une combinaison de sous-unités NR1 et de sous-unités NR2 et/ou NR3) sont des récepteurs ionotropiques activés par le glutamate et impliqués dans la toxicité excitatrice cérébrale post-ischémique. Le NGF (nerve growth factor) appartient à la classe des facteurs de croissance neurotrophiques. C’est une cytokine qui est impliquée dans la survie cellulaire et dans la neuroprotection via la voie des ERK (extracellularly regulated kinase) ou celle de la phosphatidylinositol 3-kinase (PI3K) activée par le récepteur au NGF, la tropomyosin-related kinase A (TrkA). L’électroacupuncture (EA) diminue l’expression élevée de la sous-unité NR1 et régule le niveau de TrkA chez le rat avec occlusion moyenne de l’artère cérébrale. Neuroprotection de l’EA qui est médiée par la stimulation de la voie de l’PI3-kinase, mais pas par celle des ERK [ [9] ]. AKT est une protéine kinase à sérine/thréonine qui favorise la prolifération cellulaire et la survie, s’opposant donc à l’apoptose. Cette protéine est l’acteur incontournable de la voie PI3K, une des voies majeures de conduction des signaux oncogéniques tels ceux initiés par les récepteurs EGF-R et erbB2. L’électroacupuncture aux points baihui (VG20) et renzhong (VG26) va activer la voie de survie AKT par phosphorylation de l’AKT chez le rat normal. La phospho-Akt (p-Akt) est augmentée 8h et 24h après EA au niveau du gyrus dentelé de l’hippocampe, du noyau caudé et du secteur CA1 du cortex [ [10] ].
Les facteurs de croissance sont des polypeptides ou des protéines de faible poids moléculaire qui stimulent la multiplication cellulaire des tissus. Il en existe plusieurs espèces la plupart découvertes fortuitement dans des tumeurs (TGF alpha, EGF, NGF, PDGF, IGF-1, etc..). Les TNF (tumor necrosis factor) sont aussi des facteurs de croissance pour les lymphocytes ou les fibroblastes. Ces facteurs sont reconnus par des récepteurs membranaires spécifiques qui sont le plus souvent des tyrosine kinases. Chez des chats subdivisés en cinq groupes de cinq, on sectionne partiellement et unilatéralement les ganglions des racines de la corne dorsale de la moelle épinière de L1-L5 et L7-S2, tout en épargnant L6. Les auteurs montrent que le nombre de neurones IGF1 positifs est augmenté de manière statistiquement significative (p<0,05) au niveau du ganglion dorsal de L6 dans le groupe de chats avec électroacupuncture versus le groupe sans électroacupuncture [ [11] ].Après électrostimulation de ES36 chez dix huit rats divisés en trois groupes à muqueuse gastrique à lésion stress-induite par le froid, les taux plasmatiques de prostaglandine I2 (PTGIR) étaient statistiquement augmentés alors que le TNF et le thromboxane A2 (TBXA2) étaient diminués (p<0,001) [ [12] ].
Action de l’acupuncture sur le système immunitaire
L’activité de la protéine tyrosine kinase (PTK) est augmentée par l’électroacupuncture au ES36 (zusanli) et au lanwei (point extra 33) chez des rats traumatisées au bout de 5 secondes avec un pic de réponse à 45 secondes dans la fraction sous-cellulaire des lymphocytes T activés. L’électroacupuncture contribue ainsi au signal de transduction des lymphocytes T, et prévient l’inhibition de l’activation de la PTK habituellement induite par un stress de traumatisme [ [13] ]. Dans une autre étude sur deux groupes de sept rats (Groupe EA, électroacupuncture 1,5Hz 30 mn toutes les 16 heures pendant deux jours sur 36ES ; groupe contrôle), Kim et coll. ont identifié par une technique à micromatrice d’ADN (DNA microarray technique) 154 gènes en réponse à l’EA. L’expression de l’ARNm de la PTK est augmentée de manière statistiquement significative (p<0,05) alors que celles de la protéine tyrosine phosphatase (PTP) et de la tyrosine phosphatase 1 (SHP-1) sont diminuées (elles participent à l’extinction des signaux des tyrosines kinases) entraînant une augmentation de l’activité des cellules NK (natural killers) du système immunitaire. A noter aussi l’augmentation très significative de l’expression de l’ARNm de la vascular cell adhesion molecule-1 (VCAM-1) qui est le ligand de nombreuses intégrines (ITGA4, ITGB1..) des lymphocytes B circulants mais aussi qui est exprimée dans les cellules endothéliales activées par les cytokines et régulée par l’interféron gamma (INFG) [ [14] ]. La figure 2 récapitule toutes les voies de la transduction induites par les récepteurs tyrosine kinase.
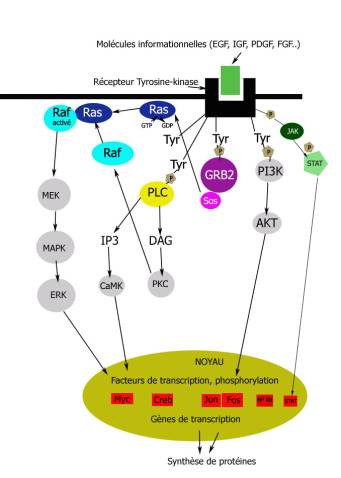
Figure 2. Les voies de transduction liées aux récepteurs à tyrosine-kinase.P : phosphate ; tyr : tyrosine ; ERK : extracellularly regulated kinase ; PI3K : phophatidylinositol-3-kinase ; CaMK : calmoduline kinase ; IP3 : inositol triphosphate ; DAG : diacylglycérol ; PKC : kinase C ; MEK : mitogen-activated protein kinase kinase ; MAPK : mitogen activated protein kinase ; GTP : guanosine triphosphate ; GDP : guanosine diphosphate ; PLC : phospholipase C ; JAK : janus kinase.
Autres récepteurs membranaires : récepteurs à cytokine
Il existe de nombreux autres récepteurs membranaires. Voici les principaux qui peuvent intervenir en acupuncture par « dowregulation » (la densité du nombre de récepteurs diminue lorsque la concentration du ligand ou molécule informationnelle extracellulaire augmente) ou par « upregulation » (à l’inverse, la densité du nombre des récepteurs augmente) : les récepteurs à cytokine : tumor necrosis factor alpha (TNF-a) [ [15] ], à interleukine 2 (IL2) [16-18], à interférons [17 ], transforming growth factor (TGF) [19,20], le nerve growth factor receptor (p75NTR ou NGFR) [21] etc..
Trente volontaires sains ont été randomisés en trois groupes de dix personnes, un groupe dit de renforcement par puncture du zusanli (36ES), un autre dit de réduction et le groupe contrôle. Dans le groupe de renforcement, le niveau de transcription de l’ARNm STAT5 a été augmenté dans les cellules mononucléaires du sang périphérique (p<0,01) alors qu’il n’y a pas de changement dans les 2 autres groupes. Les auteurs concluaient que l’action immunorégulatrice de la méthode de renforcement impliquaient les signaux de transduction des cytokines par la voie JAK/STAT [ [22] ]. La protéine STAT est phosphorylée en réponse aux facteurs de croissance et aux cytokines (interleukine 2 (IL2), IL3 etc.. et par l’intermédiaire de la kinase janus (JAK) qui a une activité de tyrosine kinase et qui est liée à la surface du récepteur à cytokine (voir figure 3).
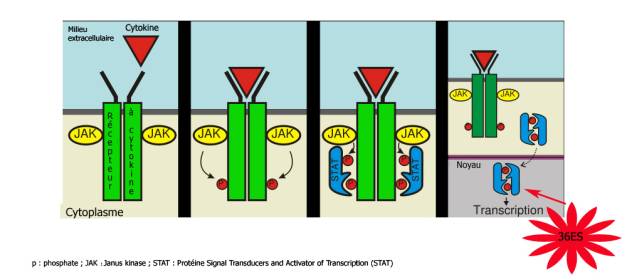
Figure 3. Action du 36ES sur les étapes de la voie de transduction des récepteurs à cytokine et la voie JAK-STAT.
NF-kappa-B (NFKB) est une protéine complexe, régulatrice de transcription, activée par de nombreux stimuli intra et extracellulaires, tels que les cytokines (TNF), les radicaux libres oxydants, les irradiations ultraviolettes etc.. La NFKB activée se transfère dans le noyau et stimule l’expression de gènes impliqués dans une grande variété de fonctions biologiques comme la réponse inflammatoire. NF-kappa-B agit sur de multiples gènes, activant prolifération et différenciation cellulaires : ostéoclastes, cellules cancéreuses, cellules vasculaires, lymphocytes, cellules bronchiques. Park et coll. ont montré que l’électroacupuncture à la fréquence de 2 et 100 Hz au 36ES entraînait une analgésie avec implication de la NFKP aussi bien dans les hautes que basses fréquences [ [23] ].
La concentration du tumor necrosis factor alpha (TNF-a) dans le sérum et le niveau de l’expression de l’ARNm du TNF-a sont augmentés de manière statistiquement significative (p<0,01) dans le groupe « rectocolite hémorragique expérimentale (RCHEx) » chez les rats non traités par acupuncture (n = 8) par rapport au groupe de rats « contrôle sans RCHEx » (n =8). L’électroacupuncture sur le zusanli (36ES) va inhiber de manière statistiquement significative (p<0,01) la TNF-a et l’ARNm du TNF-a dans le groupe RCHEx traité (n = 8). Par contre dans le groupe RCHEx traité par des non-points d’acupuncture, il n’y a pas de différence significative avec le groupe RCHEx (p>0,05) [15 ] .
L’électroacupuncture et la moxibustion ont été appliquées sur un modèle de rectocolite hémorragique (RCH) du rat afin d’étudier leurs actions sur l’apostose du polynucléaire neutrophile. Après randomisation en trois groupes (contrôle, EA, moxibustion), les auteurs ont pu constater qu’il y avait une amélioration de la RCH dans le groupe EA et moxibustion par diminution de la concentration de l’interleukine 1 bêta (IL1beta) et de IL-6 et de la TNF-alpha en rapport avec une « downregulation » des cytokines des monocytes et une apostose des neutrophiles [ [24] ].
Chez les rates présentant des ovaires polykystiques induits par du valérate d’estradiol (OPK), l’électroacupuncture module la concentration du NGF (Nerve Growth Factor) dans les ovaires [ [25] ]. Ainsi on sait que l’électroacupuncture affecte l’implication du NGF dans le dysfonctionnement ovarien [ [26] ] et normalise la NGFR dans les ovaires polykystiques induits chez les rats [21 ].
Conclusion
Les mécanismes de l’acupuncture grâce au progrès de la biologie sont de mieux en mieux connus, mais passent par une complexité croissante. Si la mécanotransduction explique la phase initiale de l’acupuncture, la réponse transductionnelle de la cellule du tissu conjonctif, que ce soit un fibroblaste, une cellule étrangère circulante (histiocytes, mastocytes, plasmocyte, lymphocyte B etc..), une cellule endothéliale ou le neurone d’un récepteur neuro-sensoriel passe par une multitude de réactions possibles et de régulations aboutissant à l’induction de protéines cibles. Cette étude montre que l’acupuncture aboutit à activer les récepteurs à tyrosine-kinase et ceux à cytokines. Nous verrons dans un prochain article que d’autres récepteurs sont concernés comme les récepteurs couplés à la protéine G ou le système impliquant les enzymes de la famille des NAD(P)H oxydases et l’intervention du monoxyde d’azote (NO).
Références
[1] . Stéphan JM. Acupuncture, tissu conjonctif et mécanotransduction. Acupuncture & Moxibustion. 2006;5(4):362-367.
[2] . Pavalko FM, Chen NX, Turner CH, Burr DB, Atkinson S, Hsieh YF, Qiu J, Duncan RL. Fluid shear-induced mechanical signaling in MC3T3-E1 osteoblasts requires cytoskeleton-integrin interactions. Am J Physiol.1998;275:C1591-601.
[3] . Sung HJ, Kim YS, Kim IS, Jang SW, Kim YR, Na DS, et al. Proteomic analysis of differential protein expression in neuropathic pain and electroacupuncture treatment models. ProteomiCoe. 2004 Sep;4(9):2805-13.
[4] . Zhou MQ, Zhou YP, Wang KM, Hu L, Wang YL, Chen YN. [Study on effects of acupuncture at the heart meridian on gene expression pattern of heart in rats with acute myocardial ischemia]. Zhongguo Zhen Jiu. 2006 Aug;26(8):587-94.
[5] . Bartolami S. Transduction du signal extracellulaire. Cours de neurobiologie Université Montpellier II. Novembre 2006 [cité 24 dec 2006]: Available from: URL: http://schwann.free.fr/transduction_du_signal.htm.
[6] . Guo JC, Gao HM, Chen J, Zhao P, Cao XD, Li Y, et al. Modulation of the gene expression in the protective effects of electroacupuncture against cerebral ischemia: a cDNA microarray study. Acupunct Electrother Res. 2004;29(3-4):173-86.
[7] . Yang ZB, Yan J, Zou XP, Yi SX, Chang XR, Lin YP, et al. Enhanced expression of epidermal growth factor receptor gene in gastric mucosal cells by the serum derived from rats treated with electroacupuncture at stomach meridian acupoints. World J Gastroenterol. 2006 Sep 14;12(34):5557-61.
[8] . Yun SJ, Park HJ, Yeom MJ, Hahm DH, Lee HJ, Lee EH. Effect of electroacupuncture on the stress-induced changes in brain-derived neurotrophic factor expression in rat hippocampus. Neurosci Lett. 2002;318(2):85-8.
[9] . Sun N, Zou X, Shi J, Liu X, Li L, Zhao L. Electroacupuncture regulates NMDA receptor NR1 subunit expression via PI3-K pathway in a rat model of cerebral ischemia-reperfusion. Brain Res. 2005 Dec 7;1064(1-2):98-107.
[10] . Wang SJ, Omori N, Li F, Zhang WR, Jin G, Hamakawa Y, et al. Enhanced expression of phospho-Akt by electro-acupuncture in normal rat brain. Neurol Res. 2002 Oct;24(7):719-24.
[11] . Liu F, Wang TH, Zhang Y, Hong SQ, Song XB. [Impact of acupuncture to IGF-I expression in spared dorsal root ganglion of cats]. Sichuan Da Xue Xue Bao Yi Xue Ban. 2006 May;37(3):384-6.
[12] . Liu Y et Al. [Proctective effect of electroacupuncture at zusanli on stress gastric mucosal damage in rats]. Journal of anhui traditional chinese medical college. 2000;19(2):27.
[13] . Cheng XD, Wu GC, He QZ, Cao XD. Effect of electroacupuncture on the activities of tyrosine protein kinase in subcellular fractions of activated T lymphocytes from the traumatized rats. Acupunct Electrother Res. 1998;23(3-4):161-70.
[14] . Kim CK, Choi GS, Oh SD, Han JB, Kim SK, Ahn HJ, et al. Electroacupuncture up-regulates natural killer cell activity Identification of genes altering their expressions in electroacupuncture induced up-regulation of natural killer cell activity. J Neuroimmunol. 2005 Nov;168(1-2):144-53.
[15] . Tian L, Huang YX, Tian M, Gao W, Chang Q. Downregulation of electroacupuncture at ST36 on TNF-alpha in rats with ulcerative colitis. World J Gastroenterol. 2003 May;9(5):1028-33.
[16] . Choi GS, Han JB, Park JH, Oh SD, Lee GS, Bae HS, et al. Effects of moxibustion to zusanli (ST36) on alteration of natural killer cell activity in rats. Am J Chin Med. 2004;32(2):303-12.
[17] . Yu Y, Kasahara T, Sato T, Guo SY, Liu Y, Asano K, et al. Enhancement of splenic interferon-gamma, interleukin-2, and NK cytotoxicity by S36 acupoint acupuncture in F344 rats. Jpn J Physiol. 1997 Apr;47(2):173-8.
[18] . Cheng XD, Wu GC, He QZ, Cao XD. Effect of continued electroacupuncture on induction of interleukin-2 production of spleen lymphocytes from the injured rats. Acupunct Electrother Res. 1997;22(1):1-8.
[19] . Chen KZ, Shi JL, Lu MZ, He ZG, Qin RA. [Effects of acupoint thread implantation and Chinese herb on PTH and TGF-beta1 in the rate of chronic renal failure]. Zhongguo Zhen Jiu. 2006 Jul;26(7):511-4.
[20] . Li R, Li WJ, Cai YN, Li ZG, Luo Q, Zhou MJ, et al. [Effects of moxibustion at Feishu (BL 13) and Gaohuang (BL 43) on expression of TGF-beta1 in the bleomycin -induced pulmonary fibrosis]. Zhongguo Zhen Jiu. 2005 Nov;25(11):790-2.
[21] . Manni L, Lundeberg T, Holmang A, Aloe L, Stener-Victorin E. Effect of electro-acupuncture on ovarian expression of alpha (1)- and beta (2)-adrenoceptors, and p75 neurotrophin receptors in rats with steroid-induced polycystic ovaries. Reprod Biol Endocrinol. 2005;3:21.
[22] . Liu ZB, Yang XH. [Effects of different manipulation methods of acupuncture at Zusanli (ST 36) on signal transduction pathway of STAT5 in human PBMC]. Zhongguo Zhen Jiu. 2006 Feb;26(2):120-2.
[23] . Park HJ, Lee HS, Lee HJ, Yoo YM, Lee HJ, Kim SA, et al. Decrease of the electroacupuncture-induced analgesic effects in nuclear factor-kappa B1 knockout mice. Neurosci Lett. 2002 Feb 22;319(3):141-4.
[24] . Wu HG, Liu HR, Tan LY, Gong YJ, Shi Y, Zhao TP, et al. Electroacupuncture and Moxibustion Promote Neutrophil Apoptosis and Improve Ulcerative Colitis in Rats. Dig Dis Sci. 2007 Jan 9.
[25] . Stener-Victorin E, Lundeberg T, Cajander S, Aloe L, Manni L, Waldenstrom U, Janson PO. Steroid-induced polycystic ovaries in rats: effect of electro-acupuncture on concentrations of endothelin-1 and nerve growth factor (NGF), and expression of NGF mRNA in the ovaries, the adrenal glands, and the central nervous system.Reprod Biol Endocrinol 2003;1(1):33.
[26] . Stéphan JM. Acupuncture expérimentale et syndrome des ovaires polykystiques. Acupuncture & Moxibustion. 2005;4(2):153-159