Résumé : Peut-on dire qu’il existe un substratum anatomique ou histologique bien spécifique et individualisé du point d’acupuncture ? Complexe neuro-vasculaire, complexe neuro-musculaire, magnétosome, théorie de Bonghan, tissu conjonctif sont les chapitres abordés par cette revue épistémologique qui conclut certes à une non individualisation d’une structure spécifique, mais propose une théorie mettant en jeu la mécanotransduction induite par les fibroblastes du tissu conjonctif, associée à l’intervention de récepteurs neuro-sensoriels. Mots-clés : Points d’acupuncture – substratum histologique – complexe neuro-vasculaire – complexe neuro-musculaire – récepteurs neuro-sensoriels – tissu conjonctif – fibroblaste – mécanotransduction – théorie de Bonghan – étude épistémologique – actine – revue.
Summary : Can one say that there is an anatomical substratum or histological good specific and individualized point of acupuncture ? Neurovascular bundles, neuromuscular attachments, magnétosome, theory of Bonghan, connective tissue are the chapters approached by this epistemological review which shows certainly non-individualization from a specific structure, but proposes a theory bringing into play the mechanotransduction induced by the fibroblasts of connective tissue, associated the intervention of sensory nerves endings. Keywords : Points of acupuncture – histological substratum – neurovascular bundles – neuromuscular attachments – sensory nerve endings – theory of Bonghan – connective tissue – fibroblast – mechanoransduction – epistemological study – actin – review.
La détermination du substratum anatomique du point d’acupuncture a ouvert la voie à de très nombreuses recherches. Dès les années 1950, Fujita remarque une analogie entre la localisation des points d’acupuncture et la topographie des éléments éruptifs des diverses maladies infectieuses comme la varicelle, la rougeole, le zona etc.. Ses observations le conduisent à noter l’apparition d’une papule au niveau du point d’acupuncture pathologique qu’il nomme « phénomène de la papule » [1]. Mais on peut considérer que la recherche du substratum anatomique a vraiment commencé avec les travaux de Bossy et Rabischong.
Les théories anatomiques ou histologiques du point d’acupuncture
Complexe neuro-vasculaire
Bossy et coll. en 1975, montraient par dissection des éléments sus-aponévrotiques que le point d’acupuncture n’avait pas une structure macroscopique spécifique. Néanmoins, un pédicule vasculo-nerveux était retrouvé dans 37% des cas, un élément vasculaire dans 34% des cas et un nerf cérébro-spinal dans 29% des cas, soit 66% d’entre eux révélaient être en rapport avec un élément nerveux [2] .
En 1975, Rabischong et coll. remarquaient que le point d’acupuncture était un point de moindre résistance électrique en relation avec une épaisseur de l’épiderme, une modification des fibres de collagène du derme associées à un paquet vasculo-nerveux entouré par un réseau de fibres amyéliniques de type cholinergique et de fibres myéliniques entrelacées [3]. En 1978, Bossy préconisait que les points d’acupuncture, microscopiquement, pouvaient être en corrélation soit avec des corpuscules nerveux de type Meissner ou Pacini, soit des fuseaux neuromusculaires ou des terminaisons nerveuses libres, soit des formations glomiques. D’un point de vue macroscopique, Bossy confirmait la variabilité des éléments situés sous le point d’acupuncture et objectivait des « espèces de cheminée de tissu conjonctif contenant des petits éléments de tissu vasculo-nerveux » [4] .
Une étude des capillaires sanguins et lymphatiques au niveau des points d’acupuncture de moindre résistivité était réalisée chez 21 lapins par la méthode électrophorétique. La lymphomicro-angiographie montrait ainsi que les points étaient surtout situés sur les capillaires lymphatiques dérivés des bouquets lymphatiques. Les auteurs pensaient que les points et les méridiens étaient en étroite relation avec les vaisseaux sanguins, les lymphatiques et les nerfs qui les contrôlent [5] .
En 1984, Bossy pensait aussi que les paquets vasculo-nerveux du derme étaient à l’origine de l’action de l’acupuncture [6] .
Odile Auziech s’était intéressée également à l’étude histologique de nombreux « points » répartis sur l’ensemble du tégument cutané, détectables grâce à leur conductance électrique sélectivement élevée, et assimilables à ceux utilisés en acupuncture. Leur détection n’était pas subordonnée à l’abondance de poils, de glandes, ni même de récepteurs spécifiques. Elle coïncidait avec la présence constante d’un agencement plus ou moins élaboré et volumineux de segments micro-vasculaires et nerveux, très réactifs et capables de transmettre des effets à distance surtout, en tant que relais sur les voies végétatives périphériques. Ces complexes furent nommée CNV pour complexe neuro-vasculaire. Pour les points d’auriculothérapie, elle notait que les observations étaient largement superposables, bien qu’avec quelques variantes [7] , [8] .
Complexes neuro-musculaires et récepteurs neuro-sensoriels
L’étude de Liu, Varela et coll. en 1975 a établi la correspondance possible entre quelques points d’acupuncture et les moto-neurones musculaires retrouvés par électromyographie à visée diagnostique. Ainsi le 4GI correspond au premier muscle interosseux dorsal de la main ; le court abducteur du pouce correspond au PO10 ; l’abducteur du petit doigt : 4TR ; 1er muscle interosseux dorsal du pied correspond au FO3 ; le muscle splenius capitis au 20VB ; le muscle sterno-cléido-mastoïdien au 18IG etc.. [9] .
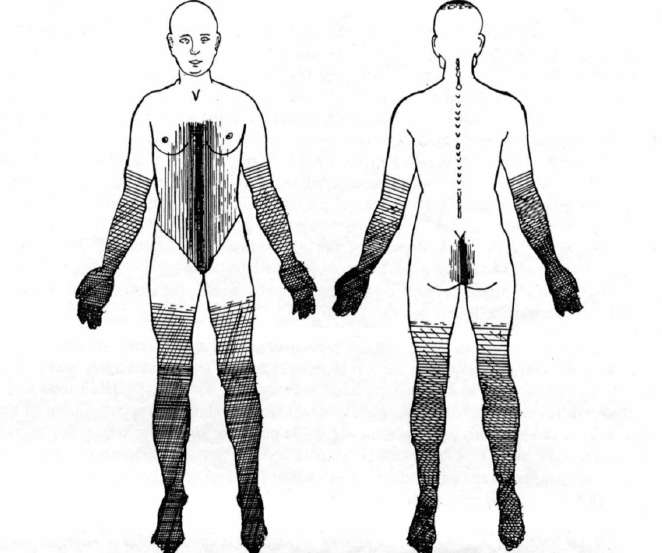
Gunn et coll. en 1976 pensaient plutôt que les points d’acupuncture étaient en relation avec des structures nerveuses sous-jacentes [10]. Plummer en 1979, après avoir fait une revue systématique des études macroscopiques et microscopiques observait la présence d’une branche d’un nerf sous-cutané au niveau de très nombreux points [11]. Dung en 1984, suite à ses études anatomiques sur le cadavre jugeait aussi que le point d’acupuncture était localisé à la terminaison d’une branche neuro-musculaire des différents nerfs du corps humain. Il décrivit de cette façon tous les points d’acupuncture et les replaça sur les trajets des différentes branches neuro-musculaires. Pour cet auteur, les nerfs crâniens étaient par exemple le substratum anatomique des points d’acupuncture du crâne. Au Vème nerf trijumeau, par l’intermédiaire de ses différentes branches ophtalmique, maxillaire et mandibulaire correspondrait ainsi la plupart des points d’acupuncture de Vessie, Estomac, Vésicule Biliaire (figure 1) etc.. [12]. Même chose pour tous les autres points d’acupuncture du reste du corps, avec les branches des plexus brachial, cervical, thoracique, lombaire ou sacré [13-17].
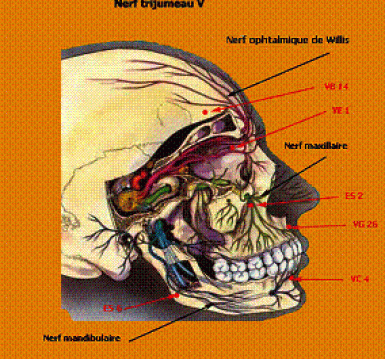
Figure 1. Correspondance entre quelques points d’acupuncture et les différentes branches du nerf trijumeau.
Une étude a identifié la présence de récepteurs sensoriels musculaires chez le singe au niveau du 36ES, 4GI associé à des fibres myélinisées de grand calibre [18]. Une autre étude chinoise en 1996 sur le 6RP objective de multiples structures à la fois nerveuses, sanguines et lymphatiques mais sans que cela soit statistiquement significatif [19] .
En 1983, Lu et coll. ont montré que l’activité du point 36ES (zusanli) était corrélée par la distribution de nombreuses afférences de fibres myélinisées du groupe III (Aδ) et surtout du groupe II (fibres Aγ et essentiellement fibres Aβ) [20] .
Li et coll. en 2004 [21] ont montré que les fibres A alpha, bêta, delta et les fibres C se terminent par des récepteurs sensoriels cutanés ou musculaires dont la distribution est étroitement associée à celle des points d’acupuncture. Cela a été mis en évidence sur les pattes postérieures de rats par corrélation entre la distribution des terminaisons nerveuses et les points d’acupuncture. Au niveau de la peau, les terminaisons nerveuses se concentrent essentiellement soit sur les sites des points d’acupuncture ou le long des méridiens. Chez vingt-sept rats, les auteurs objectivèrent que les récepteurs sensoriels musculaires (fuseaux neuro-musculaires, récepteurs de Golgi des ligaments articulaires, mécanorécepteurs sensibles à la pression) ou les récepteurs sensoriels cutanés (fibres Aβ, Aδ et fibres C) étaient localisés sur le trajet du méridien de Vessie et celui de Rate-Pancréas ainsi que préférentiellement sur les points Hors Méridiens EX-LE12 au niveau des orteils. Les auteurs suggéraient que les points d’acupuncture pouvaient être des complexes neuro-cutanéo-musculaires à haute densité de terminaisons nerveuses. Kagitani et coll. confirment en 2005 ces différents travaux en montrant que la stimulation manuelle de 36ES chez le rat activait les quatre types de fibres du groupe I à IV, mais nettement moins le groupe IV [22].
En 2005, Xi et coll. injectèrent au point d’acupuncture 20VB (refu) un soluté à 30% de peroxydase de raifort (PR) chez cinquante rats Wistar aléatoirement divisés en 5 groupes de 10 animaux. Des sections de 40 μm des ganglions spinaux cervicaux, de la moelle épinière cervicale et thoracique et du cerveau ont été étudiés après incubation et teinture au rouge neutre. Les auteurs retrouvèrent des neurones positifs au PR dans les régions bilatérales ou homonymes du 1er au 4ème ganglion médullaire cervical, de la 1ère à la 4ème corne antérieure de la moelle cervicale, la division ventromédiale du noyau facial et accessoirement du noyau facial ipsilatéral. De ce fait, les auteurs concluaient que par corrélation, le 20VB avait son effet en rapport avec la branche postérieure auriculaire du nerf facial, la branche antérieure des 2ème et 3ème nerfs cervicaux et des 1ère au 4ème cornes antérieures cervicales de la moelle épinière, de la division ventromédiale de noyau facial et du noyau facial accessoire [23] .
Le magnétosome
Moal a découvert des amas métalliques de cristaux de magnétite (Fe304), les magnétosomes, aux points d’acupuncture [24] . La taille de ces magnétosomes est comparable à celle des virus, c’est à dire 500 Angström. Ces cristaux représentent un système de type condensateur électrique et/ou parallèlement une réserve de type » coenzyme métallique » nécessaire à toute réaction enzymatique et seraient présents de façon naturelle chez tous les individus. Moal explique que chez l’homme, le point d’acupuncture serait une réserve naturelle d’énergie, une sorte de pile ou de batterie pouvant être rechargée extérieurement par la stimulation de l’aiguille d’acupuncture. Les prélèvements opérés pour cette recherche ont été effectués sur des cadavres frais (personnes décédées depuis 24 heures environ) à la morgue du CHU de Brest. Sur les points d’acupuncture GI4, FO3, ES36, ont été prélevés superficiellement des morceaux de derme de 6 à 8mm de diamètre. Afin de les comparer aux points d’acupuncture, des points en dehors des méridiens ont également été prélevés et étudiés. Sur les trente prélèvements (dont 15 hors-méridiens) et après coloration au Perls (le fer ferrique présent dans les tissus réagit avec le ferrocyanure de potassium) ou à l’Hémalin Eosine Safran (HES), cinq se sont révélés positifs à la coloration de Perls avec apparition des grains de Fe3O4 en amas de couleur noire dispersés et nombreux sur les coupes d’histologie classique et en couleur jaune orange ambré à l’HES. Ces grains étaient présents dans le derme autour des glandes sudoripares. Les magnétosomes ont déjà été décrits essentiellement chez les bactéries et permettraient aux organismes vivants de s’orienter dans le temps et dans l’espace [25] , [26] . Par contre, il n’existe aucune autre étude permettant de confirmer l’existence des magnétosomes au point d’acupuncture.
Le réseau de Bonghan
Dans les années 1960, en Corée, Bonghan Kim a proposé la théorie de Bonghan pour expliquer la structure histologique des points et des méridiens d’acupuncture [27]. Il a décrit que les points d’acupuncture étaient des corpuscules contenant des granules Sanal connectés à des structures filiformes intravasculaires : le réseau de Bonghan. Il s’agit d’un réseau de conduits parcourant tout l’organisme, en surface et en profondeur. Ces conduits sont intravasculaires, voire extravasculaires et constitués eux-mêmes d’un faisceau de canalicules dont la paroi est faite d’une assise de cellules endothéliales et dont la lumière contiendrait un liquide circulant différent du sang ou de la lymphe et particulièrement riche en acide désoxyribonucléique [1 ].
Tissu conjonctif
Certains auteurs ont suggéré une correspondance entre les points d’acupuncture et le tissu conjonctif, en particulier les fibres de collagène qui pourraient servir de voies de conduction pour les communications à travers tout le corps [28]. Déjà en 1987, Kimura et coll. observaient au microscope électronique l’action de la pénétration de l’aiguille dans le tissu conjonctif de rats, mais aussi par moxibustion. Il révélait une augmentation de la présence du nombre de lymphocytes, monocytes, mastocytes, polynucléaires neutrophiles et éosinophiles, davantage d’ailleurs des suites de la moxibustion que de l’acupuncture [29]. Rappelons que ces cellules mobiles sont partie intégrante du derme au même titre que les fibroblastes. Les mêmes auteurs en 1992 s’intéressaient à l’effet de la manipulation de l’aiguille à la recherche du deqi. L’analyse au microscope électronique révélait une atteinte du tissu conjonctif : fibres de collagène, fibres élastiques, fibroblastes, mastocytes et adipocytes étaient enroulés autour de l’aiguille dans le prélèvement recueilli et étudié sur la peau d’un volontaire. Par contre, les structures nerveuses étaient rarement observées. Ils en déduisaient qu’une relation fonctionnelle possible entre manipulation de l’aiguille et induction du deqi pouvait être responsable de la constitution anatomique du point d’acupuncture[30]. En 1996, une équipe chinoise observait au microscope que l’induction du deqi au point zusanli (36ES) chez le cobaye entraînait un enroulement des fibres du tissu conjonctif avec transformation et dislocation des structures neuro-vasculaires adjacentes. Les auteurs en concluaient que le tissu conjonctif devait être le médiateur et la base biologique de l’acupuncture [31] .
Cette relation par l’intermédiaire du deqi entre points d’acupuncture, méridiens et tissu conjonctif servit de base aux travaux de l’équipe de Langevin, à partir de 2001 [32-35].
On le sait, la recherche du deqi est l’élément essentiel pour avoir un effet thérapeutique par acupuncture, et selon Langevin, c’est vraisemblablement une des clefs permettant la compréhension de son mécanisme d’action. La recherche du deqi est cette technique très particulière qui se présente sous deux composantes : une sensation plus ou moins douloureuse et désagréable perçue par le patient et la sensation de saisissement et de blocage de l’aiguille par la peau perçue par l’acupuncteur.
Cependant, il est à noter que les travaux espagnols d’Abad-Alegría montre, à partir de potentiels évoqués somesthésiques déclenchés par la stimulation progressive jusqu’à la sensation du deqi au GI4 (hegu), que l’effet de stimulation de l’acupuncture est en rapport avec l’intensité du stimulus appliqué. D’autre part, la sensation de deqi n’est pas une condition sine qua none pour obtenir des modifications neuro-fonctionnelles, mais malgré tout, c’est avec une recherche efficace du deqi que les effets acupuncturaux seront les meilleurs [36].
Langevin et al. formulèrent l’hypothèse que les effets locaux et distants de l’acupuncture peuvent s’expliquer par ce phénomène bio-mécanique. Le saisissement de l’aiguille est du à un couplage mécanique entre l’aiguille et le tissu conjonctif qui s’enroule autour d’elle. De ce fait la manipulation de l’aiguille transmet, via le signal mécanique déclenché par les cellules du tissu conjonctif, une mécanotransduction qui engendre à son tour une modification du milieu intra et extra-cellulaire avec tout son cortège de neuromodulation.
Comment Langevin et al. ont démontré cette théorie ?
Ils ont utilisé un extraordinaire appareil de puncture assisté par ordinateur et servomoteurs qui a permis de puncturer, manipuler, retirer l’aiguille de manière automatique, tout en ayant la possibilité de programmer la profondeur, la vitesse de rotation. Soixante volontaires ont été étudiés avec randomisation en trois groupes : groupe NO, absence de manipulation ; groupe BI, 16 rotations alternées bi-directionnelles (horaire – antihoraire) ; groupe UNI, 16 rotations dans un seul sens unidirectionnel, horaire. 16 points ont été étudiés, 8 points d’acupuncture (4GI, 36ES, 6PO, 6RP, 2CO, 32VB, 11GI, 57VE), et 8 non-points situés à 2 ou 3 cm des précédents. La profondeur de puncture a été déterminée par échographie en fonction de l’épaisseur du tissu cutané de chaque point et adaptée à chaque sujet. Grâce à toute cette procédure, il est mis en évidence une augmentation de la force nécessaire au retrait de l’aiguille de 167% en cas de manipulation horaire (groupe UNI) et de 52% dans le groupe BI, comparé au groupe NO. Par ailleurs, il existe une différence statistiquement significative (p<0,001) de 18% entre points d’acupuncture et non-points, bien que cette différence soit moins importante que celle entre manipulation et non manipulation [32].
Tout cela suggère une relation étroite entre manipulation de l’aiguille par recherche du deqi et déclenchement des événements biomécaniques en rapport avec le tissu conjonctif.
L’étape suivante pour Langevin et al. a été de démontrer que cette force de retrait du au deqi était bien en rapport avec le tissu conjonctif plutôt qu’avec une contraction du muscle. Ils l’ont démontré en mesurant la force de retrait de l’aiguille avec ou sans pénétration du muscle par contrôle échographique chez 60 volontaires âgés de 18 à 55 ans. Langevin et coll. ont utilisé le même protocole décrit précédemment avec le même type d’appareil. Deux localisations ont été définies : une située en région lombaire (tissu musculaire), et l’autre en région sacrée (tissu conjonctif). A été observée de manière statistiquement significative (p<0,05) une augmentation de la force de retrait des aiguilles plantées dans le tissu conjonctif par rapport à celles pénétrant le muscle, et cela davantage élevée dans le groupe UNI (manipulation unidirectionnelle) que dans les autres groupes (NO et BI). Une autre partie de l’étude a consisté à étudier les coupes histologiques de tissu conjonctif prélevées sur la peau de 13 rats ayant bénéficié de l’insertion d’aiguilles, suivie ou non d’une recherche du deqi avec rotation unidirectionnelle. Les coupes histologiques ont révélé une augmentation statistiquement significative (p<0,001) de tissu conjonctif enroulé autour de l’aiguille dans le groupe avec rotation horaire par rapport à celui sans manipulation [33].
Une autre étude toujours des mêmes auteurs a constaté l’effet de cette manipulation de l’aiguille. Sur les coupes histologiques de tissu conjonctif prélevé sur la peau de rats, on observe une déformation nette de la matrice du tissu conjonctif qui prend un aspect spiralé autour de l’emplacement de l’aiguille (figure 2). Le réseau de fibres collagène et élastique de la matrice extracellulaire est déformé en tourbillon, le tout associé à une augmentation du nombre de fibroblastes dont le cytosquelette s’épaissit par polymérisation des filaments d’actine G (globulaire) en actine F (filamenteuse). Ces observations suggèrent que le signal mécanique créé par la manipulation de l’aiguille induit donc des réarrangements du cytosquelette du fibroblaste et également dans les autres cellules présentes dans le tissu conjonctif, tels les cellules endothéliales des capillaires [ 34 ].
En 2002, Langevin et al ont formulé une nouvelle théorie audacieuse : les méridiens et les points d’acupuncture peuvent être vus comme une représentation du réseau formé par le tissu conjonctif interstitiel. Cette hypothèse fut soutenue par des images ultrasoniques montrant les plans de clivage du tissu conjonctif aux points d’acupuncture chez les sujets humains normaux. Pour évaluer cette hypothèse, les auteurs ont étudié les points d’acupuncture dans les sections anatomiques du bras humain post-mortem. Ils ont trouvé une correspondance de 80% entre les sites des points d’acupuncture et l’emplacement des plans de clivage de tissus conjonctifs intermusculaires ou intramusculaires [35 ].

Figure 2. Vue d’artiste de l’aspect spiralé autour de l’emplacement de l’aiguille, d’après l’image ultrasonique microscopique de Langevin [34 ].
Déjà, dans un article précédent, Langevin et coll. avaient démontré que le phénomène de saisissement de l’aiguille se voyait aussi bien sur les points d’acupuncture que les non-points, bien que la force de retrait était inférieure de 18% chez ces derniers. Ce qui peut sembler logique, étant donné que le tissu conjonctif est réparti à tous les niveaux du corps humain. Il restait donc à trouver pour quelle raison certains points avaient un effet de saisissement plus élevé. Langevin et coll. ont ainsi étudié les coupes anatomiques au niveau du bras. La localisation des points d’acupuncture pour les six méridiens du bras est retrouvée dans 80% des cas au niveau ou à l’intersection des plans de clivage du tissu conjonctif, tout en éliminant la probabilité du facteur chance. Et il paraît évident que des résultats similaires peuvent être obtenus au niveau des autres régions du corps, du thorax au membre inférieur où d’ailleurs, ils retrouvent par exemple un autre plan de clivage visualisé à l’échographie au point VB32, mais non visible sur un point contrôle situé à 3 cm sur le muscle vaste latéral [34].
La sensation de la propagation du deqi, très souvent décrite par les auteurs pourrait s’expliquer aussi comme une réponse des mécanorécepteurs à la stimulation de l’aiguille, entraînant à distance une vague de contraction du tissu conjonctif par l’intermédiaire vraisemblable de la polymérisation de l’actine des fibroblastes.
Langevin et coll. se sont largement étendus dans toutes leurs publications sur les mécanismes sous-tendant les effets physiologiques de l’acupuncture.
Pour eux, l’acupuncture n’aura un effet que par la recherche du deqi. La rotation unidirectionnelle de l’aiguille délivre un signal mécanique par saisissement de l’aiguille, réorganisation du tissu conjonctif en spirale autour de l’aiguille, entraînant alors une réponse cellulaire et une mécanotransduction.
En 2004, Langevin et coll. ont alors étudié les changements du cytosquelette du fibroblaste engendrés par l’étirement du tissu cellulaire sous-cutané. Cela va entraîner un large éventail de réactions cellulaires incluant mécanotransduction, expression de gène et adhérence de matrice extracellulaire par les points d’adhésion focaux. Bien que l’importance des forces mécaniques sur la forme et la fonction de cellules soit bien établie sur les cellules en culture, on connaît très peu les effets sur les tissus in vivo. Dans cette étude, l’étirement de 25% de tissu sous-cutané de souris ex-vivo (pendant 10 minutes à 2 h) a engendré une augmentation temps-dépendante significative du périmètre de corps du fibroblaste et de son aire de section transversale (p<0,01). Au bout de 2 heures, l’aire de section transversale du corps du fibroblaste était 201% plus grand dans le tissu étiré que dans celui non étiré. Les fibroblastes dans le tissu étiré avaient un corps plus grand, en forme de feuille avec des prolongements plus courts, les lamellipodes. En revanche, les fibroblastes dans le tissu non étiré présentaient une morphologie « dendritique » avec un corps cellulaire plus globuleux et de plus longs processus. In vivo, on observe la même chose au bout de 30 minutes. Ex vivo, ces transformations sont inhibées par la colchicine et la cytochalasine D, ce qui prouve que les microtubules et les microfilaments d’actine en sont responsables [37]. L’effet entre les microtubules et les microfilaments peut également contribuer à la « contraction » apparente des corps des fibroblastes lors de la rétraction du tissu. Les changements morphologiques du cytosquelette des fibroblastes ont des implications importantes dans les signaux intracellulaires de type paracrine ou autocrine au niveau du tissu conjonctif [38].
La rotation de l’aiguille d’acupuncture engendre une stimulation mécanique provoquant une réponse physiologique, la mécanotransduction, par remodelage du cytosquelette des fibroblastes du tissu conjonctif sous-cutané. Cette mécanotransduction entraîne une cascade complexe de réactions intra et extracellulaires, incluant l’activation de la phosphorylation de la « mitogen activated proteine kinases » (MAP kinase), de la « focal adhesion kinase » (FAK) et de la « extracellular signal-regulated signal » (ERK). Langevin et coll. ont étudié sous microscopie confocale l’effet de la rotation de l’aiguille d’acupuncture par analyse morphométrique des explants de tissu sous-cutanés ( 8cm sur 3cm) de six souris sacrifiées. Cette rotation d’aiguille induit l’étalement du fibroblaste en forme de feuille et la formation de lamellipodes (c’est un prolongement avec aplatissement du cytoplasme lors d’un déplacement) dans un délai de 30 minutes mesurable par l’accroissement de l’aire de section du corps cellulaire. L’effet de la stimulation acupuncturale est à son apogée avec deux rotations et diminue de manière statistiquement significative (p<0,001) à 4, 8 ou 12 rotations. Les effets significatifs de la rotation s’observent dans tout le tissu et montre son extension de plusieurs centimètres. Tout est bloqué par les inhibiteurs pharmacologiques de la contractilité de l’actinomyosine (blebbistatine), de la Rho-kinase (Y-27632 et H-1152), et de la protéine Rac-1. En conclusion, en réponse à une rotation d’une aiguille d’acupuncture, il a enroulement et attraction du tissu de la périphérie vers l’aiguille attirant la matrice extracellulaire vers les fibroblastes aux points de contacts focaux (ce sont les plaques d’adhérence focale sur lesquelles opèrent les récepteurs transmembranaires : les intégrines) existants, puis formation de lamellipodes (Rac induit) dans les régions de la cellule qui sont mécaniquement stimulées ; augmentation de la contraction de l’actinomyosine (Rho-induite) sans formation de fibres distinctes de stress ; migration de microtubule et stabilisation ; augmentation de la tension intracellulaire, expansion du fibroblaste et aplatissement en un tissu plat jusqu’à atteindre une nouvelle tension d’équilibre (actinomyosine-induite) avec deux types de forces opposées (issue de la matrice extracellulaire et celle de la compression intracellulaire en rapport avec l’expansion du cytosquelette). Par contre, on n’observe pas d’action de la JNK-2 qui est un important médiateur de l’apostose et de l’activation de certains gènes [39].
Dans une autre étude en 2006, Langevin et coll poursuivaient leurs travaux sur l’étirement du tissu conjonctif et observaient la distribution de l’α et β-actine dans les fibroblastes du tissu sous-cutané ex-vivo. Les fibroblastes normaux exposent uniformément une immunoréactivité alpha-actine des muscles lisses (alpha-SMA). En cas d’étirement du tissu, ces fibroblastes n’auront pas de forme F-actine, ni d’organisation en fibres distinctes de stress. Le manque de fibres de stress et de complexes de type fibronexus a été confirmé par la microscopie électronique, indiquant que ces cellules fibroblastiques observées dans le tissu étiré n’étaient pas des myofibroblastes. Dans le tissu non étiré, l’alpha-actine est diffuse et granulaire. Après un étirement de 30 minutes, l’α-actine a formé une structure en forme d’étoile centrée par le noyau suggérant la formation de fibres de stress mais sans la classique polymérisation de l’actine, alors que la β-actine se prolongeait dans tout le cytoplasme incluant le cortex cellulaire et les lamellipodes. Cette réponse duale de l’alpha et bêta-actine peut être un composant majeur des mécanismes cellulaires de la mécanotransduction appliquée au tissu conjonctif entraînant une restructuration du cytosquelette du fibroblaste. Le fibroblaste a ainsi développé tout un répertoire de réponse à un stress mécanique : un stress de court terme (quelques minutes à heures comme l‘insertion d’une aiguille d’acupuncture) entraîne une redistribution de l’alpha et bêta-actine et un rapide remodelage du cytosquelette qui peut donc jouer un rôle important dans la régulation de la tension du tissu conjonctif. Au contraire, la réponse des fibroblastes à un stress mécanique de long terme (jours à semaines) et une blessure va provoquer l’accroissement de la synthèse d’alpha-actine et la transformation en myofibroblaste [40].
Ifrim et coll. en 2005 [41] ont réalisé une étude histologique sur les points d’acupuncture. Cent dix personnes souffrant d’hémiplégie ont été divisés en deux groupes traités par électroacupuncture. Le groupe I a bénéficié d’une électroacupuncture des points GI11, GI15, GI4, ES36, ES43, RP5, VB34 et VB39. Le groupe II a été traité par GI8, GI10, ES32, ES8 et VB38. Des biopsies ont été prises sur ces différents points, fixés et teintés à la coloration éosine hématotoxyline et au PAS. Le traitement électroacupunctural a été plus efficace dans le groupe I par rapport au groupe II. Les auteurs ont montré après une étude histologique et anatomique comparative que les points du groupe I qui semblent plus efficaces sur l’hémiplégie, bénéficiaient d’une haute densité de fines fibres nerveuses, d’un réseau capillaire bien développé et d’une concentration accrue en mucopolysaccharides (MPS), en particulier, les mucopolysaccharides acides. Malheureusement, cette étude n’est pas crédible du fait d’une méthodologie et d’une métrologie totalement insuffisantes avec aucune étude statistique permettant d’évaluer l’étude.
Les mêmes auteurs [42] ont alors réalisé une autre étude dans le but d’élucider les spécificités structurales des points d’acupuncture et des méridiens. Ils ont étudié 356 prélèvements. Les échantillons ont été biopsiés à trois niveaux différents : le groupe 1 avec prélèvement sous les points d’acupuncture (IG7, FO8, VG13, ES36) ; le groupe 2 le long des méridiens de Triple Réchauffeur, de Rate-Pancréas, du Vaisseau Gouverneur ; le groupe 3 à distance des méridiens. Les auteurs ont constaté que dans le groupe 1 les points d’acupuncture étaient associés à une haute densité de tissu conjonctif, de mucopolysaccharides (MPS), en particulier de la MPS acide, associé à une abondance de fibres de collagène et de terminaisons nerveuses. Par contre pas de changement de concentration en fibres réticulaires et élastiques. De telles concentrations étaient encore marquées dans le groupe 2, mais nettement moins dans le groupe 3.
Cette étude est intéressante, car confirme ce que les études de Langevin avaient observé, tout en ignorant totalement ces travaux. Néanmoins, comme la précédente, ce travail souffre encore d’un manque de rigueur expérimentale.
Substratum des structures anatomiques du point d’acupuncture
Au terme de cette analyse bibliographique, il s’avère qu’aucune étude ne démontre de manière irréfutable l’existence d’un substratum bien individualisé anatomique ou histologique du point d’acupuncture, que ce soit par l’existence d’un complexe neuro-vasculaire de type CNV, d’un complexe neuro-musculaire, d’un magnétosome ou d’un corpuscule de Bonghan.
Le principal problème auquel on se heurte ici est la reproductibilité des observations et une méthodologie insuffisante. Dans la plupart de ces études, il manque de nombreuses données dans la description de l’expérience. On doit faire confiance à l’expérimentateur, ce qui n’est pas un comportement scientifique. C’est pourtant le premier intérêt d’une publication : rendre accessible à la critique une expérience qui doit pouvoir être reproductible. L’analyse statistique constitue, habituellement, une part importante d’une étude expérimentale ou clinique, même si elle ne suffit pas à apprécier l’intérêt du résultat obtenu. Un bon jugement scientifique est également nécessaire qui dépend à la fois de la précision de sa description, de sa mesure, mais aussi de ses conditions d’observation, car la crédibilité d’un fait observé est liée aux conditions dans lesquelles l’étude a été réalisée. La notion de mesure fait fréquemment appel aux statistiques. Aucune de ces études ne fit état des analyses statistiques permettant de comparer les points d’acupuncture versus non-points d’acupuncture.
Heureusement, quelques travaux dont essentiellement ceux de Langevin et coll. s’avèrent satisfaire à toutes les contraintes d’une étude expérimentale scientifique. Le point d’acupuncture se situerait donc à l’emplacement des points de clivage du tissu conjonctif lâche inter ou intramusculaire. L’action acupuncturale se ferait par l’intermédiaire de la recherche du deqi, avec rotation de l’aiguille qui engendre une mécanotransduction, faisant intervenir les molécules informationnelles libérées par la déformation du cytosquelette du fibroblaste. Celle-ci entraînerait aussi par la déformation de la matrice extracellulaire du tissu conjonctif une stimulation des différents types de récepteurs neuro-sensoriels avec activation des différentes fibres nerveuses appartenant aux groupes I à IV, déclenchant à leur tour une cascade de réactions aussi bien au niveau local qu’au niveau du système nerveux central. En conclusion, ce modèle pourrait servir de nouveau paradigme tout à fait plausible et vraisemblable au concept de substratum anatomique du point d’acupuncture (figure 3).
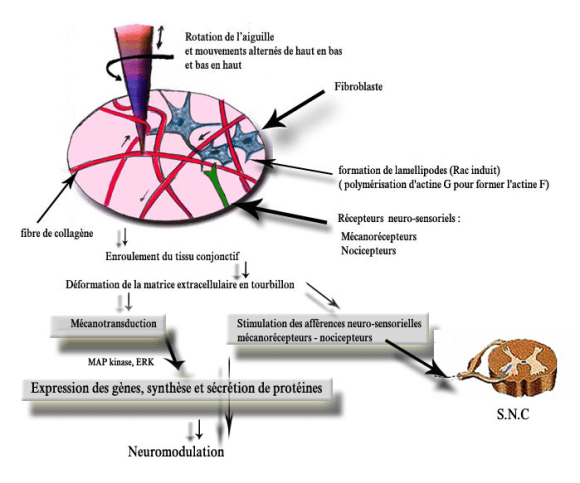
Figure 3. Schéma récapitulatif du paradigme du substratum du point d’acupuncture avec intervention du tissu conjonctif.

Réferences
[1] . Briot A, Wong M. Histoire de l’acupuncture sino-japonaise. Méridiens. 1974;25-26:15-55.
[2] . Bossy J, Maurel JC, Godlewski. Substratum macroscopique des points d’acupuncture. Bulletin de l’association des anatomistes. 1975;59(165):357-62.
[3] . Rabischong P, Niboyet JE, Terral C, Senelar R, Casez R. Bases expérimentales de l’analgésie acupuncturale. Nouv Presse Med. 1975;4(28):2021-6.
[4] . Bossy J. Les différents points d’acupuncture : leurs caractères, leur répartition et leurs liaisons avec les structures connues. Méridiens. 1978;41-42:73-95.
[5] . Gong Qihua. [Structure vasculaire du point d’acupuncture déterminé par microradiographie (méthode électrophorétique)]. Zonghua Yixue Zazhi. 1979;59(8):476-8.
[6] . Bossy J. Morphological data concerning the acupuncture points and channel network. Acupunct Electrother Res. 1984;9(2):79-106.
[7] . Auziech O. Etude histologique des points cutanés de moindre résistance électrique et analyse de leurs implications possibles dans la mise en jeu des mécanismes acupuncturaux. Thèse Médecine. Montpellier: 1984.
[8] . Senelar R, Auziech O. Histophysiologie du point d’acupuncture. Acupuncture et Médecine Traditionnelle Chinoise, Paris. Encyclopédie des Médecines Naturelles. 1989;1B-2C.
[9] . Liu Y, Varela M, Oswald R. The correspondence between some motor points and acupuncture loci. Am J Chin Med (Gard City N Y). 1975 Oct;3(4):347-58.
[10] . Gunn CC, Ditchburn FG, King MH, Renwick GJ.Acupuncture loci: a proposal for their classification according to their relationship to known neural structures. Am J Chin Med. 1976;4(2):183-95.
[11] . Plummer JP. Acupuncture points and cutaneous nerves.Experientia. 1979;35(11):1534-5.
[12] . Dung HC. Acupuncture points of the cranial nerves.Am J Chin Med. 1984;12(1-4):80-92.
[13] . Dung HC.Acupuncture points of the cervical plexus.Am J Chin Med.1984;12(1-4):94-105.
[14] . Dung HC. Acupuncture points of the brachial plexus.Am J Chin Med. 1985;13(1-4):49-64.
[15] . Dung HC. Acupuncture points of the typical spinal nerves.Am J Chin Med.1985;13(1-4):39-47.
[16] . Dung HC. Acupuncture points of the sacral plexus. Am J Chin Med. 1985;13(1-4):145-56.
[17] . Dung HC. Acupuncture points of the lumbar plexus.Am J Chin Med. 1985;13(1-4):133-43.
[18] . Ha H. et al. Receptors in acupuncture point in the monkey (résumé)]. anatomical record. 1983;205(3),71A.
[19] . Yu A et al. [observation on the microsstricture of sanyinjiao acupoint]. Acupuncture research. 1996,21(2),36-8.
[20] . Lu GW. Characteristics of afferent fiber innervation on acupuncture points zusanli. Am J Physiol. 1983 Oct;245(4):R606-12.
[21] . Li AH, Zhang JM, Xie YK. Human acupuncture points mapped in rats are associated with excitable muscle/skin-nerve complexes with enriched nerve endings. Brain Res. 2004 Jun 25;1012(1-2):154-9.
[22] . Kagitani F, Uchida S, Hotta H, Aikawa Y. Manual acupuncture needle stimulation of the rat hindlimb activates groups I, II, III and IV single afferent nerve fibers in the dorsal spinal roots. Jpn J Physiol. 2005 Jun;55(3):149-55.
[23] . Xi GM, Wang HQ, He GH, Huang CF, Yuan QF, Wei GY, et al. Nerve-pathways of acupoint Fengch’ih in rat by anterograde transport of HRP. World J Gastroenterol. 2005 May 28;11(20):3135-8.
[24] . Moal P. Recherche en microscopie électronique et à la microsonde d’une structure particulière du point d’acupuncture : le magnétosome. Applications thérapeutiques. Actes du V° Congrès de la FAFORMEC; 2001 30 nov.-1 déc ; Nantes. Available from: URL: http://www.acupuncture-medic.com/Congres/Nantes/magnetosome.htm
[25] . Bazylinski DA, Frankel RB, Heywood BR, Mann S, King JW, Donaghay PL, et al. Controlled Biomineralization of Magnetite (Fe(inf3)O(inf4)) and Greigite (Fe(inf3)S(inf4)) in a Magnetotactic Bacterium. Appl Environ Microbiol. 1995 Sep;61(9):3232-9.
[26] . Grunberg K, Muller EC, Otto A, Reszka R, Linder D, Kube M, et al. Biochemical and proteomic analysis of the magnetosome membrane in Magnetospirillum gryphiswaldense. Appl Environ Microbiol. 2004 Feb;70(2):1040-50.
[27] . Kim B. On the Kyungrak systeme. Medical Science Press, Pongyang, Korea,1963.
[28] . Ho MW, Knight DP. The acupuncture system and the liquid crystalline collagen fibers of the connective tissues. Am J Chin Med. 1998;26(3-4):251-63
[29] . Kimura M, Mastrogiovanni F, Toda S, Kuroiwa K, Tohya K, Sugata R, Ohnishi M. An electron microscopic study of the acupuncture or moxibustion stimulated regional skin and lymph node in experimental animals. Am J Chin Med. 1988;16(3-4):159-67.
[30] . Kimura M, Tohya K, Kuroiwa K, Oda H, Gorawski EC, Hua ZX, Toda S, Ohnishi M, Noguchi E. Electron microscopical and immunohistochemical studies on the induction of « Qi » employing needling manipulation.Am J Chin Med. 1992;20(1):25-35.
[31] . Shi X, Zhang Q.[Dynamic study of tissues and structures in « de qi » acupoint] Zhen Ci Yan Jiu. 1996;21(3):60-2.
[32] . Langevin HM, Churchill DL, Cipolla MJ. Mechanical signaling through connective tissue: a mechanism for the therapeutic effect of acupuncture. Faseb J. 2001 Oct;15(12):2275-82.
[33] . Langevin HM, Churchill DL, Fox JR, Badger GJ, Garra BS, Krag MH. Biomechanical response to acupuncture needling in humans. J Appl Physiol. 2001 Dec;91(6):2471-8.
[34] . Langevin HM, Churchill DL, Wu J, Badger GJ, Yandow JA, Fox JR, et al. Evidence of connective tissue involvement in acupuncture. Faseb J. 2002 Jun;16(8):872-4.
[35] . Langevin HM, Yandow JA. Relationship of acupuncture points and meridians to connective tissue planes. Anat Rec. 2002 Dec 15;269(6):257-65.
[36] . Abad-Alegría F, Pomaron C, Barcala-Simo MA. Control de la somestesia por estimulo neuroreflejo : cuantificación de estímulo-respuesta frente a energía. Rev Neurol. 2003;37(5):421-5.
[37] . Langevin HM, Bouffard NA, Badger GJ, Iatridis JC, Howe AK. Dynamic fibroblast cytoskeletal response to subcutaneous tissue stretch ex vivo and in vivo. Am J Physiol Cell Physiol. 2005 Mar;288(3):C747-56.
[38] . Kessler D, Dethlefsen S, Haase I, Plomann M, Hirche F, Krieg T, et al. Fibroblasts in mechanically stressed collagen lattices assume a « synthetic » phenotype. J Biol Chem. 2001 Sep 28;276(39):36575-85.
[39] . Langevin HM, Bouffard NA, Badger GJ, Churchill DL, Howe AK. Subcutaneous tissue fibroblast cytoskeletal remodeling induced by acupuncture: Evidence for a mechanotransduction-based mechanism. J Cell Physiol. 2006 May;207(3):767-74.
[40] . Langevin HM, Storch KN, Cipolla MJ, White SL, Buttolph TR, Taatjes DJ. Fibroblast spreading induced by connective tissue stretch involves intracellular redistribution of alpha- and beta-actin. Histochem Cell Biol. 2006 May;125(5):487-95.
[41] . Ifrim-Chen F, Ifrim M. The relation between the acupoint structures and the clinical therapeutic effects. Ital J Anat Embryol. 2005 Jan-Mar;110(1):45-9.
[42] . Ifrim-Chen F, Ifrim M. Acupoints [corrected] and meridians: a histochemical study. Ital J Anat Embryol. 2005 Jan-Mar;110(1):51-7.
Stéphan JM. A la recherche du substratum anatomique du point d’acupuncture. Acupuncture & Moxibustion. 2006;5(3):252-261. (Version 2006)