Résumé : Outre son activation de l’axe neuro-endocrinien et du système limbique, le stress va déclencher une libération en cascade de molécules informationnelles engendrant des pathologies psycho-somatiques invalidantes, tels les gastrites, ulcères et hypertension artérielle. L’acupuncture permettra de reconstituer un système naturellement protecteur, essentiel à la vie relationnelle. L’acupuncture expérimentale offre des réponses physiopathologiques à l’action acupuncturale qui agit en particulier par des mécanismes de transduction cellulaire intervenant sur les interleukines, prostaglandines, monoxyde d’azote, oxyde nitrique synthase, EGF, CGRP, dopamine, sérotonine et bêta-endorphine. Mots-clés: acupuncture expérimentale – revue – stress – transduction cellulaire – molécules informationnelles – EGF – interleukine – NO – NOS – CGRP – dopamine –sérotonine –bêta-endorphine.
Summary : In addition to its activation of the hypothalamo-pituitary-adrenal axis and limbic system, the stress will start a release in cascade of informational molecules generating of invalidating psycho-somatic pathologies, such as gastritis, ulcers and arterial hypertension. Acupuncture will make it possible to reconstitute a naturally protective system, essential with the relational life. Experimental acupuncture offers physiopathological answers to the acupuncture action which acts in particular by mechanisms of cellular transduction intervening on interleukins, prostaglandins, nitric oxide synthase, NO, EGF, CGRP, dopamin, serotonin and beta-endorphin. Keywords: experimental acupuncture – review – stress – cellular transduction – informational molecules – EGF – interleukin – NO – NOS – CGRP – dopamine – serotonin – beta-endorphin.
Depuis qu’Hans Selye a établi le concept du « stress » en 1936, sur la base d’expérimentations réalisées chez le rat, et décrit les lésions gastriques comme l’une des trois entités anatomopathologiques qui définissent un syndrome de stress avec l’augmentation de la taille des surrénales et l’atrophie du thymus, on sait que l’organisme réagit aux différents types d’agressions physiques, psychiques ou environnementales, survenant sur un mode aigu ou chronique, en mettant en jeu ses propres moyens de défense. Nous avons vu l’action de l’électroacupuncture sur l’axe neuro-endocrinien et le système limbique dans le précédent numéro. La transduction cellulaire est un autre mécanisme d’action privilégié de l’acupuncture par l’intermédaire des molécules informationnelles comme les interleukines, les prostaglandines, monoxyde d’azote (NO), EGF (epidermal growth factor), peptide relié au gène de la calcitonine (CGRP), dopamine, sérotonine et bêta-endorphine.

Stress et transduction cellulaire : les molécules informationnelles impliquées
Les organismes pluricellulaires doivent conserver leur homéostasie. Les informations, au minimum un signal, c’est-à-dire une information simple concernant un état de l’organisme ou un événement interne ou externe font intervenir les mécanismes de transduction. Les corps chimiques qui transmettent les informations les moins complexes, simples signaux, sont qualifiés de molécules informationnelles (molécules-signaux). Ces molécules sont produites par des cellules qui ont une information à transmettre. Puis, elles sont diffusées dans la cellule elle-même (effet autocrine), vers les cellules voisines (effet paracrine) ou sécrétées dans le milieu intérieur, voire à l’extérieur (effet hormonal). Ensuite, elles sont reconnues par les cellules qui reçoivent ce signal et le traitent pour le traduire en un effet prédéterminé. Les molécules informationnelles appartiennent à toutes les classes de corps chimiques : dérivés d’acides aminés (cathécolamines, GABA), alcools dérivés des phospholipides (acétyl-choline..), nucléosides et nucléotides, eicosanoïdes (prostaglandines et thromboxanes etc..), stéroïdes, stérols (stéroïdes, aldostérone, cortisol, progestérone, oestradiol, testostérone etc..), sans oublier les nombreux peptides (insuline, opioïdes, neurohormones, hormones digestives) ou les hormones ou stimulines, protéines ou glycoprotéines complexes (stimulines, immunoglobulines, hormones, facteurs de croissance). Ces molécules informationnelles sont vraisemblablement un des fondements de l’acupuncture. En voici quelques unes principalement concernées dans le stress.
Interleukine 2
Elle est généralement diminuée en cas de stress. L’IL-2 joue un rôle important dans la régulation du système immunitaire en assurant la stimulation générale de l’immunité cellulaire, activant les cellules lymphocytaires et macrophagiques en permettant la différenciation des lymphocytes T en lymphocytes NK dont le nombre pourra donc être aussi diminué [1]. L’interleukine 2 favorise ainsi spécifiquement la multiplication des lymphocytes T cytotoxiques. Elle est capable de stimuler la prolifération des lymphocytes T4 (CD4) et des lymphocytes T8 (CD8), l’activité des macrophages et la production d’anticorps par les lymphocytes B. Cependant, comme pour les cellules NK, en fonction du stress, on pourra avoir soit une augmentation ou une diminution de l’interleukine 2. Ainsi le stress par rotation stimule la synthèse de l’ARNm de l’IL-2 dans les lymphocytes alors qu’elle sera inhibée de 30% lors d’un stress par immobilisation chez le rat [2] .
Prostaglandines
Les prostaglandines, prostacyclines, thromboxanes et leucotriènes sont des dérivés de l’acide arachidonique. La voie de la cyclo-oxygénase conduit à la formation de la prostaglandine H2. En fonction de la machinerie enzymatique de la cellule où elle est formée, la prostaglandine H2 sera transformée soit en thromboxane A2 , en prostacycline (PGI2), en prostaglandine F2a (PGF2a) , ou encore en prostaglandine E2 (PGE2). Au niveau de l’estomac, la PGE2 et la PGI2 jouent un rôle protecteur important en inhibant la sécrétion acide et en stimulant la production locale de mucus protecteur. Les plaquettes sanguines forment de la thromboxane A2, laquelle joue un rôle important dans la coagulation sanguine en favorisant l’agrégation des plaquettes. Un excès de thromboxane A2 favorise la formation des thrombi qui obstruent les vaisseaux. En cas de gastrite ou d’ulcère en rapport avec un stress, les prostaglandines PGE2 et PGI2 seront de manière statistiquement significative diminuées [3] . Chez le rat stressé, l’apport de PGEI va alors prévenir les lésions de la muqueuse gastrique [4] .
Oxyde nitrique synthase et monxyde d’azote (NO)
Des lésions gastriques sont induites par un stress d’immersion pendant 6 heures dans l’eau. Il est observé outre les lésions gastriques, une diminution importante de 1’oxyde nitrique synthase, facteur d’exacerbation des lésions gastriques. La synthèse du monoxyde d’azote, NO ou oxyde nitrique s’effectue à partir de la L-arginine grâce à la NO-synthase. On distingue trois types d’isoenzymes NO-synthases : l’isoenzyme de type I (NOS1), présente dans les neurones et les cellules épithéliales, l’isoenzyme de type II (NOS2), présente dans différents types de cellules, dont les macrophages, après induction par les cytokines, et l’isoenzyme de type III (NOS3), présente essentiellement dans les cellules endothéliales. De nombreux travaux ont démontré que le NO peut avoir à la fois des propriétés protectrices ou délétères vis-à-vis de la muqueuse gastrique lors d’un stress. Cela dépend du NOS impliqué. Ainsi, la NOS2, apparaît dans les macrophages, les neutrophiles et les hépatocytes sous l’influence de cytokines, notamment l’interleukine-1, du Tumor Necrosis Factor etc.. L’induction de cette NO-synthase par effet génomique nécessite un délai de plusieurs heures mais la NO-synthase induite est immédiatement active après sa synthèse et entraîne une libération prolongée et très importante de NO. Les NOS2 et 3 entraînent un processus d’ulcère gastrique en cas de stress au froid alors que le NOS1 en permettant de synthétiser davantage de NO a un effet protecteur de la muqueuse gastrique. Le monoxyde d’azote (NO), d’abord mis en évidence dans l’endothélium vasculaire est le principal facteur vasodilatateur libéré par la cellule endothéliale tapissant tout l’arbre vasculaire, artères et veines, du cœur jusqu’aux capillaires. Le NO entraîne donc une relaxation des fibres vasculaires lisses, une bronchodilatation, un relâchement de l’estomac après le repas pour l’adapter au contenu alimentaire et une inhibition de l’agrégation plaquettaire et de l’adhésion des plaquettes à l’endothélium [5] .
EGF (epidermal growth factor) et peptide relié au gène de la calcitonine (CGRP)
L’ARNm de l’epidermal growth factor (EGF) est augmenté au niveau de l’hypophyse en cas de stress par le froid ou à l’immobilisation et joue un rôle important dans la libération d’ACTH [6]. Par contre, le taux d’EGF est diminué dans la muqueuse gastrique en cas de lésion stress-dépendante par le froid ou l’immobilisation. L’EGF doit son rôle gastro-protecteur à son action sur l’élévation des prostaglandines [7] . De même le stress par l’immersion dans l’eau entraîne une diminution du peptide relié au gène de la calcitonine (CGRP) induisant une gastrite chez le rat [8] .
Dopamine et sérotonine
La dopamine possède une fonction gastro-intestinale modulatrice et a des activités anti-sécrétoires et gastroprotectrices comme cela a été démontré chez le rat, mais en fonction des récepteurs [9] . Une DOPA décarboxylase produit la dopamine, qui est ensuite oxydée en noradrénaline, puis méthylée en adrénaline. Plusieurs types de récepteurs à dopamine ont été caractérisés dans la substance noire, les tubercules olfactifs ou le noyau caudé, ainsi que dans l’hypophyse. En cas de stress par immersion chez le rat, la dopamine sera augmentée mais si le récepteur dopaminergique est de type D2, l’action sera gastro et duodéno-ulcérigène, par contre si la dopamine se fixe sur les récepteurs D1, son action sera gastro-protectrice [10] .
En cas de stress d’immobilisation chez le rat, la sérotonine (5-hydroxytryptamine, 5-HT) est aussi augmentée au niveau du noyau hypothalamique paraventriculaire (PVN) [11] .
Action sur le système immunitaire et sur l’inflammation
Effet pro-inflammatoire
Le stress peut modifier la distribution et la prolifération de certaines cellules immunitaires [12] , l’activité des macrophages, des cellules NK (Natural Killer) et des lymphocytes T [13] . Ainsi, le stress réduit le nombre de cellules NK intraparenchymateuses pulmonaires via l’activation des récepteurs bêta adrénergiques [14] mais pourra aussi dans d’autres conditions, comme un stress par rotation [15] augmenter les cellules NK plasmatiques, les lymphocytes tout en diminuant la proportion des lymphocytes T CD3+, CD4+ (acteurs de la réponse acquise de type cellulaire) et lymphocytes B CD19+ (responsables de la réponse acquise de type humoral) [16] .
Différents peptides et protéines produits par le système immunitaire, tels que les interleukines et les interférons, possèdent des fonctions hormonales. Chez les animaux, des situations de stress comme une unique session de chocs électriques, une exposition à une nage forcée dans de l’eau froide etc.. accroissent la production de cytokines inflammatoires comme l’interleukine-1b (IL-1b) ou l’interleukine-6 (IL-6) par les cellules de la rate, les macrophages péritonéaux et les macrophages pulmonaires [17-19] ainsi que la Substance P (neurotransmetteur appartenant à la famille des neurokinines (NK) synthétisées par la cellule nerveuse au niveau du locus niger et de la glande pinéale).
L’interleukine-1b et l’interleukine-6 peuvent aussi par rétrocontrôle stimuler la libération d’ACTH et de CRH, mais aussi de bêta endorphines. Les catécholamines sont impliquées dans cette production de cytokines inflammatoires. La voie de transcription du facteur nucléaire kB (NF-kB) est l’une des principales voies intracellulaires responsables de l’expression de cytokines inflammatoires. Chez l’homme, un stress aigu active la voie NF-kB dans les cellules mononucléées sanguines (lymphocytes, macrophages, et monocytes) et induit l’expression des gènes nucléaires de ces cellules qui en dépendent, ayant pour conséquence la production de cytokines [20] . La noradrénaline pourrait être responsable de cette activation puisqu’elle est en mesure d’activer la voie NF-kB des monocytes sanguins. Le stress exacerbe aussi les réponses de type inflammatoire en induisant la libération locale de CRH par les terminaisons nerveuses périphériques en potentialisant ensuite la libération de facteur de nécrose tumoral (TNF-a), d’IL-1b et d’IL-6 par les macrophages [21] .
Effet anti-inflammatoire
Outre l’effet pro-inflammatoire, le stress peut aussi exercer un effet anti-inflammatoire qui résulte principalement de l’action des glucocorticoïdes qui en se liant au facteur de transcription NF-kB va empêcher l’activation de la transcription de cytokines inflammatoires.
L’effet pro ou anti-inflammatoire du stress dépend du type de stress. Ainsi chez la souris, si une infection par le virus de la grippe ou un stress psychosocial à type de réorganisation sociale favorisent la réponse inflammatoire dans les poumons, un stress de contention répété a l’effet inverse [22] , [23] . La figure 1 résume les différentes actions du stress sur le système hypothalamo-hypophyso-surrélanien que nous avions décrit dans un précédent article ainsi que celles sur le système immunitaire et inflammatoire et ces différentes interactions.
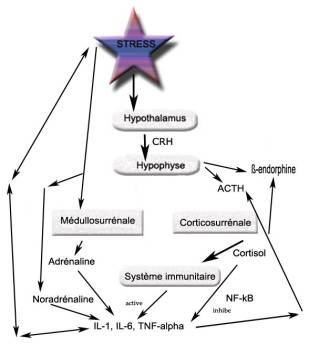
Figure 1. Principales actions du stress sur l’axe neuro-endocrine, le système immunitaire et inflammatoire et sa régulation.
Action de l’acupuncture sur le stress
Système gastro-intestinal
Chez des rats, une équipe russe a démontré que l’effet de l’électroacupuncture était comparable à celui de 2,5mg/kg de diazépam et entraînait une réduction significative des érosions gastriques et de la réactivité au stress par rapport au groupe témoin [24] .
Cinquante septs rats Sprague Dawley ont été soumis à des stress associant 170 rotations/mn en étant lié ou un stress engendré par l’exposition au froid (0-4 degrés C, 30-60 minutes). Les auteurs ont utilisé les points d’acupuncture ES36 (zusanli) et VE21 (weishu). 63,2% des rats stressés ont développé des lésions de la muqueuse gastro-intestinale visualisées au microscope à type d’hyperémie ou d’hémorragie réparties sur 15,8 à 27,7% de la muqueuse. Dans le groupe acupuncture et stress, 16,7% des rats seulement ont objectivé des hémorragies ou de l’hyperémie atteignant 1,7% de la muqueuse [25] .
Des rats Wistar ont été divisés en deux groupes, groupe acupuncture et groupe contrôle. Par immersion et immobilisation des rats dans l’eau, on a induit un ulcère gastrique de stress. L’action de l’électroacupuncture réduit l’ulcération peptique. L’électroacupuncture inhibe la synthèse de la sérotonine (la sérotonine a une action ulcérigène et son administration à l’animal à fortes doses entraîne des ulcérations gastriques) alors que les taux de noradrénaline sont plus élevés au niveau du cortex, de l’hypothalamus et du tronc cérébral et dans le sang par rapport au groupe contrôle, mais moins élevés au niveau du tissu gastrique avec inhibition de la gastrine. De même, la dopamine est augmentée dans le sang et le tissu gastrique chez les rats traités par électroacupuncture (notons que la dopamine a un effet inhibiteur de la motricité digestive) [26] , [27] . Chez des rats Sprague Dawley, un modèle de stress a été induit par leur immersion dans l’eau froide à 4° pendant 30-40 mn. L’action de l’acupuncture appliquée à ES36 (zusanli) a été étudiée par l’activité électrique gastro-entérique. On observe ainsi des effets inhibiteurs de l’activité électrique gastro-colique chez les rats stressés par l’application de l’acupuncture au zusanli [28] .
Après électrostimulation de ES36 chez dix huit rats divisés en trois groupes à muqueuse gastrique à lésion stress-induite par le froid, les taux plasmatiques de prostaglandine I2 (PGI2) ont été statistiquement augmentés alors que le TNF (tumor necrosis factor : action inflammatoire) et le thromboxane A2 (TXA2) ont été diminués (p<0,001) [29] .
Quatre-vingt-seize rats Sprague Dawley males ont été divisés aléatoirement en groupe témoin, groupe sous stress psychologique et groupe stress traité par électroacupuncture afin de déterminer l’amélioration des désordres gastriques stress-dépendants. Zusanli (ES36) a été puncturé et stimulé électriquement pendant 30 minutes. L’activité électrique du noyau dorsal moteur du nerf vague a été enregistrée. Après stimulation acupuncturale les anomalies provoquées par le stress ont été régulées par action sur le nerf pneumogastrique (une hyperactivité du nerf X entraîne outre une tendance aux syncopes et à l’anxiété, une constipation, une hyperchlorhydrie, un myosis etc..) [30] (voir figure 2).
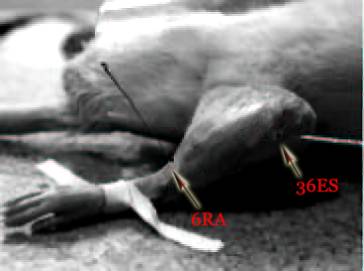 Figure 2. Localisation du point ES36 au niveau de la patte du rat par rapport au RA6 sur la face antéro-interne de la patte. |
On a étudié les effets de l’électroacupuncture du point zusanli (ES36) sur l’EGF (epidermal growth factor) et le peptide relié au gène de la calcitonine (CGRP : inhibiteur aussi de la sécrétion gastrique) chez les rats stressés. Quarante rats Wistar ont été divisés aléatoirement en plusieurs groupes, groupe témoin de 8 rats, un groupe stress (n=8) et un groupe stress traité par électroacupuncture, subdivé en 3 sous-groupes en fonction de la durée du traitement électroacupunctural : 1, 3 et 5 jours. La méthode d’immobilisation dans le froid a été considérée comme le modèle de stress. On a observé sous différents microscopes les changements structurels de la muqueuse gastrique. Par rapport au groupe contrôle, l’EGF et le CGRP plasmatique diminuent de manière statistiquement significative (p<0,05) dans le groupe stress. Dans les groupes traités acupuncturalement, les taux plasmatiques d’EGF et de CGRP s’accroissent significativement (p<0,01) et davantage dans le groupe traité pendant 5 jours. Par ailleurs, les nécroses et altérations de la muqueuse gastrique et de l’endothélium vasculaire étaient plus graves dans le groupe stress que dans ceux traités par acupuncture. On a noté aussi que le degré d’amélioration est fonction de la durée de traitement [31] . Une autre étude chinoise en 2001 confirme encore l’action de l’acupuncture de manière statistiquement significative (p<0,01) dans les gastrites stress-induites chez le rat Wistar en inhibant les lésions dues aux radicaux libres tels le malondialdehyde (marqueur de stress oxydatif) et en augmentant dans le plasma et la muqueuse gastrique l’activité de la dismutase du superoxyde (SOD), une des enzymes responsables des mécanismes de résistance des cellules au stress oxydatif [32] .
Vingt deux rats mâles Sprague Dawley ont été randomisés en 3 groupes : groupe contrôle (n=6), groupe stress (n=8), et groupe pré-acupuncture (n=8). Le groupe stress était soumis à un stress par le froid pendant 1 heure après avoir été anesthésié. Le groupe pré-acupuncture bénéficiait d’un traitement électroacupunctural au zusanli (ES36) pendant 1 semaine à raison de 30 mn par jour, avant d’être soumis au stress par le froid. Après sacrifice de l’animal, les auteurs ont étudié l’expression du NOS (oxyde nitrique synthase) au niveau de l’hypothalamus et de la glande surrénale puis mesuré la concentration du cortisol plasmatique et l’effet protecteur éventuel de l’acupuncture sur la muqueuse gastrique. Les résultats montrent une décroissance significative des lésions ulcéreuses, une diminution de la concentration plasmatique du cortisol chez les rats bénéficiant de l’acupuncture. L’expression de la NOS1 dans l’hypothalamus est significativement augmentée après acupuncture alors que celle des NOS2 et 3 est diminuée. Au niveau des surrénales, l’expression de la NOS3 qui augmente après exposition au stress de froid, est diminuée seule par l’acupuncture au ES36. Pas de changement pour NOS1 et 2 [33] . La figure 3 résume l’action de l’acupuncture sur le système gastro-intestinal.
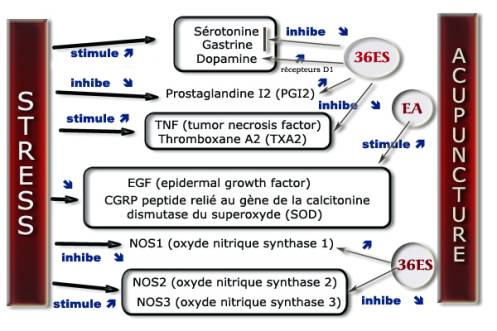
Figure 3. Effets du stress et de l’acupuncture sur le système digestif.
Système immunitaire
L’EA contribue aussi au signal de transduction transmembranaire des lymphocytes T en rapport avec le stress et permet aux récepteurs transmembranaires à activité tyrosine-kinase de constituer une cible de la plupart des facteurs de croissance ou cytokines. Ainsi l’électroacupuncture des points zusanli (ES36) et lanwei (point hors méridien 33) empêche l’inhibition de l’activation de la tyrosine protéine kinase (TPK) dans les fractions sous-cellulaires des lymphocytes T activés des rats stressés par traumatisme [34] . De même l’EA au niveau de ces mêmes points induit chez les rats stressés par traumatisme la production d’interleukine IL-2 par les lymphocytes de la rate et améliore de ce fait l’immunosuppression provoquée par le stress [35] . En utilisant les mêmes points d’acupuncture, Du et coll confirmeront que l’immunosuppression est réduite par induction de l’interleukine 2 et inhibition des cellules NK par l’intermédiaire du système des peptides opioïdes endogènes, car inhibé par la naloxone, antagoniste des récepteurs à endorphines [36] .
Six points du Vaisseau Conception (renmai) ont été puncturés dans le but de connaître leur action sur l’activité des cellules NK et de l’interleukine 2 (cytokine IL-2). Des souris ont été randomisées : un groupe « témoin » (n = 15), un groupe « stress sans acupuncture » (n = 15), un groupe « stress avec manipulation des aiguilles » (n = 15) et un groupe « stress avec électroacupuncture » (n = 15). Les points RM17 (shanzhong), RM18 (yutang), RM19 (zigong), RM20 (huagai), RM21 (xuanji) et RM22 (tiantu) ont été stimulés pendant 20 minutes. Le traitement a été conduit quotidiennement pendant 10 jours, puis intervalle d’une semaine entre deux séries thérapeutiques. Après 3 séries de traitement, les auteurs ont observé que dans le groupe « stress sans acupuncture » au niveau de la rate et du thymus des souris, l’activité des cellules NK et de l’IL-2 était diminuée de manière statistiquement significative par rapport au groupe « témoin », alors que dans les deux autres groupes traités par acupuncture, les variables étudiées étaient significativement plus élevées (p<0,05) par rapport au groupe « stress sans acupuncture ». L’acupuncture augmente donc les activités des cellules de NK et d’IL-2 chez des souris soumises au stress [37] .
Sur un paradigme de stress chirurgical chez le rat, Zhao et coll. ont montré qu’il y avait amplification de l’activité des macrophages péritonéaux avec augmentation de l’interleukine 1 (IL-1) et avec d’autre part, inhibition de l’orphanine FQ au niveau du système nerveux central. On sait que la nociceptine, appelée auparavant orphanine FQ, est une protéine neuropeptide de 17 acides aminés, ayant des similarités avec la dynorphine A. Elle agit sur des récepteurs appelés ORL-1 (opioid receptor like-1). Elle module la perception douloureuse, la réduisant ou l’augmentant selon les conditions expérimentales. L’EA sur les points ES36 (zusanli) et lanwei (hors méridien 33, 2 cun sous ES36) améliore la réponse des cellules du système immunitaire, va activer la nociceptine et diminuer l’activité de l’IL-1 bêta [38] . La figure 4 récapitule l’action de l’acupuncture sur le système immun.
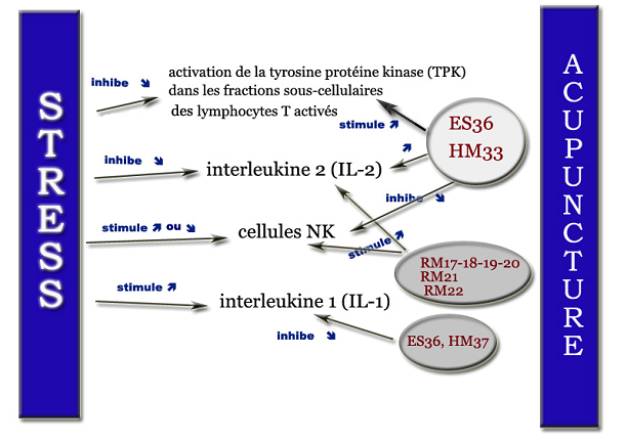
Figure 4. Stress, acupuncture et système immun.
Autre action : sur l’HTA stress-induite
Un modèle de rat hypertendu a été réalisé par stress chronique (bruits et décharges électriques aux pattes). Sur de tels rats hypertendus, une fois anesthésiés à l’uréthane et la chloralose, l’électroacupuncture aux points bilatéraux zusanli (ES36) pendant 20 minutes a eu pour conséquence un abaissement des pressions systolique et diastolique associé à une bradycardie ainsi que d’une atténuation de la pression ventriculaire systolo-diastolique gauche. L’EA avec microinjection de N(omega) – Nitro- L-Arginine, inhibiteur de la synthèse d’oxyde nitrique (NO) dans la substance grise périaqueducale ventrale (vPAG) a eu pour effet une réduction voire suppression de l’action de l’électroacupuncture sur le cœur de manière stastistiquement significative. Ces résultats suggèrent que l’effet dépresseur de l’EA sur les rats hypertendus stress-induits pourrait être en rapport avec l’oxyde nitrique ou monoxyde d’azote (NO) synthétisé dans le vPAG avec activation du système inhibiteur sympathique [39] . Il a d’ailleurs été démontré que la stimulation des points MC5 (jianshi) et MC6 (neiguan) chez le chat réduit la réponse sympathique à travers un mécanisme opioïde impliquant les récepteurs opioïdes δ et μ (forte affinité avec les bêta-endorphines et les enképhalines) dans le noyau RVLM (rostral ventrolateral medulla) du bulbe rachidien [40] mais aussi au niveau de la substance grise périaqueductale ventro-latérale (vlPAG) [41] . Chao et coll. [42] avaient d’ailleurs déjà en 1999 démontré cela en faisant des micro-injections de naloxone dans le noyau RVLM (rostral ventrolateral medulla) chez les chats bénéficiant aussi d’une électroacupuncture au MC6. Cela eût pour effet de lever l’effet inhibiteur de la réponse du système nerveux sympathique. Ce qui signifie que l’électroacupuncture au MC6 active les récepteurs opioïdes spécialement localisés dans le noyau RVLM. Celui-ci est formé de plusieurs groupes de neurones dont les projections excitatrices rejoignent la corne latérale de la substance grise de la moelle où sont situés les corps cellulaires des neurones sympathiques préganglionnaires.
En conclusion, il s’avère qu’en cas de stress, les points d’acupuncture n’agissent pas uniquement sur l’axe hypothalamo-hypophyso-surrénalien et la libération principale de CRH (corticotropin-releasing hormone) comme nous l’avons vu dans un précédent article [43], mais mettent en jeu des phénomènes de transduction avec ses nombreuses molécules informationnelles.
Références
[1] . Abraham E. Effects of stress on cytokine production. Methods Achiev Exp Pathol 1991;14:45-62.
[2] . Korneva EA, Barabanova SV, Golovko OI, Nosov MA, Novikova NS, Kazakova TB. C-fos and IL-2 gene expression in rat brain cells and splenic lymphocytes after nonantigenic and antigenic stimuli. Ann N Y Acad Sci 2000;917:197-209.
[3] . Gitlin N, Ginn P, Kobayashi K, Arakawa T. The relationship between plasma cortisol and gastric mucosa prostaglandin levels in rats with stress ulcers. Aliment Pharmacol Ther 1988;2(3):213-20.
[4] . Harada N, Okajima K, Murakami K, Isobe H, Liu W. Gastric prostacyclin (PGI2) prevents stress-induced gastric mucosal injury in rats primarily by inhibiting leukocyte activation. Prostaglandins Other Lipid Mediat 1999;57(5-6):291-303.
[5] . Goto H, Tachi K, Hisanaga Y, Kamiya K, Ohmiya N, Niwa Y, et al. Exacerbatory mechanism responsible for water immersion stress-induced gastric lesions in aged rats compared with young rats. Clin Exp Pharmacol Physiol 2001;28(8):659-62.
[6] . Fan X, Nagle GT, Collins TJ, Childs GV. Differential regulation of epidermal growth factor and transforming growth factor-alpha messenger ribonucleic acid in the rat anterior pituitary and hypothalamus induced by stresses. Endocrinology 1995;136(3):873-80.
[7] . Aricioglu A, Oz E, Erbas D, Gokcora N. Effects of EGF and allopurinol on prostaglandin and lipid peroxide levels in mucosa of stomach in restraint cold stress. Prostaglandins Leukot Essent Fatty Acids 1996;54(4):285-8.
[8] . Evangelista S, Renzi D. A protective role for calcitonin gene-related peptide in water-immersion stress-induced gastric ulcers in rats. Pharmacol Res 1997;35(4):347-50.
[9] . Glavin GB, Hall AM. Central nervous system and gut interactions: dopamine and experimental gastroduodenal lesions. J Gastroenterol Hepatol 1994;9 Suppl 1:S36-9.
[10] . Desai JK, Goyal RK, Parmar NS. Characterization of dopamine receptor subtypes involved in experimentally induced gastric and duodenal ulcers in rats. J Pharm Pharmacol 1999;51(2):187-92.
[11] . Garrido MM, Fuentes JA, Manzanares J. Gastrin-releasing peptide mediated regulation of 5-HT neuronal activity in the hypothalamic paraventricular nucleus under basal and restraint stress conditions. Life Sci 2002;70(25):2953-66.
[12] . Dhabhar FS. Stress-induced enhancement of cell-mediated immunity. Ann N Y Acad Sci 1998;840:359-72.
[13] . Kusnecov AW, Rabin BS. Stressor-induced alterations of immune function: mechanisms and issues. Int Arch Allergy Immunol 1994;105(2):107-21.
[14] . Kanemi O, Zhang X, Sakamoto Y, Ebina M, Nagatomi R. Acute stress reduces intraparenchymal lung natural killer cells via beta-adrenergic stimulation. Clin Exp Immunol 2005;139(1):25-34.
[15] . Hale KD, Ghanta VK, Gauthier DK, Hiramoto RN. Effects of rotational stress of different duration on NK cell activity, proinflammatory cytokines, and POMC-derived peptides in mice. Neuroimmunomodulation 2001;9(1):34-40.
[16] . Isowa T, Ohira H, Murashima S. Immune, endocrine and cardiovascular responses to controllable and uncontrollable acute stress. Biol Psychol 2005.
[17] . Starkie RL, Hargreaves M, Rolland J, Febbraio MA. Heat stress, cytokines, and the immune response to exercise. Brain Behav Immun 2005;19(5):404-12.
[18] . Zhu GF, Chancellor-Freeland C, Berman AS, Kage R, Leeman SE, Beller DI, et al. Endogenous substance P mediates cold water stress-induced increase in interleukin-6 secretion from peritoneal macrophages. J Neurosci 1996;16(11):3745-52.
[19] . Persoons JH, Moes NM, Broug-Holub E, Schornagel K, Tilders FJ, Kraal G. Acute and long-term effects of stressors on pulmonary immune functions. Am J Respir Cell Mol Biol 1997;17(2):203-8.
[20] . Bierhaus A, Wolf J, Andrassy M, Rohleder N, Humpert PM, Petrov D, et al. A mechanism converting psychosocial stress into mononuclear cell activation. Proc Natl Acad Sci U S A 2003;100(4):1920-5.
[21] . Elenkov IJ, Chrousos GP. Stress Hormones, Th1/Th2 patterns, Pro/Anti-inflammatory Cytokines and Susceptibility to Disease. Trends Endocrinol Metab 1999;10(9):359-368.
[22] . Sheridan JF, Stark JL, Avitsur R, Padgett DA. Social disruption, immunity, and susceptibility to viral infection. Role of glucocorticoid insensitivity and NGF. Ann N Y Acad Sci 2000;917:894-905.
[23] . Konstantinos AP, Sheridan JF. Stress and influenza viral infection: modulation of proinflammatory cytokine responses in the lung. Respir Physiol 2001;128(1):71-7.
[24] . Andreev BV, Vasil’ev Iu N, Ignatov Iu D, Kachan AT, Bogdanov NN. [Effect of electroacupuncture on signs of emotional stress caused by pain]. Biull Eksp Biol Med 1981;91(1):18-20.
[25] . Xiang L, Zhu F, Ma Y, Weng E, Tang G. [Influences of acupuncture on gastroduodenal mucosal lesion and electrical changing induced by stress in rats]. Zhen Ci Yan Jiu 1993;18(1):53-7.
[26] . Shen D, Liu B, Wi D, Zhang F, Chen Y. [Effects of electroacupuncture on central and peripheral monoamine neurotransmitter in the course of protecting rat stress peptic ulcer]. Zhen Ci Yan Jiu 1994;19(1):51-4.
[27] . Shen D, Wei D, Liu B, Zhang F. [Effects of electroacupuncture on gastrin, mast cell and gastric mucosal barrier in the course of protecting rat stress peptic ulcer]. Zhen Ci Yan Jiu 1995;20(3):46-9.
[28] . Xu G. [Influence of stress on gastroenteric electric activity and modulated effect of acupuncture on it in rats]. Zhen Ci Yan Jiu 1994;19(2):72-4.
[29] . Liu Y et Al. [Proctective effect of electroacupuncture at zusalnli on stress gastric mucosal damage in rats]. Journal of anhui traditional chinese medical college 2000;19(2):27.
[30] . Wang J et Al. [Experimental study on the effect of electroacupuncture in ameliorating gastric motor disorders under psychological stress in rats]. Acupuncture Research 2000;25(4):267.
[31] . Ming Q et Al. Effect of electroacupuncture of zusanli on plasma EGF, CGRP and gastric mucosa in stress rats. World Journal of acupuncture-moxibustion 2001;11(2):31.
[32] . Xuefei W, Junjiang Z, Yongming G et Al. [Experimental study on preventive effect of warning-dredging needling methods on stress lesion of gastric mucosa in rats]. Chinese acupuncture and moxibustion 2001;21(10):609.
[33] . Sun JP, Pei HT, Jin XL, Yin L, Tian QH, Tian SJ. Effects of acupuncturing Tsusanli (S(T)36) on expression of nitric oxide synthase in hypothalamus and adrenal gland in rats with cold stress ulcer. World J Gastroenterol 2005;11(32):4962-6.
[34] . Cheng XD, Wu GC, He QZ, Cao XD. Effect of electroacupuncture on the activities of tyrosine protein kinase in subcellular fractions of activated T lymphocytes from the traumatized rats. Acupunct Electrother Res 1998;23(3-4):161-70.
[35] . Cheng XD, Wu GC, He QZ, Cao XD. Effect of continued electroacupuncture on induction of interleukin-2 production of spleen lymphocytes from the injured rats. Acupunct Electrother Res 1997;22(1):1-8.
[36] . Du LN, Jiang JW, Wu GC, Cao XD. Naloxone and electroacunpunture (EA) improve the immune function of traumatized rats. Sheng Li Xue Bao 1998;50(6):636-42.
[37] . Hong Y, Lirong Y, Huifang M et Al. [Effects of acupuncture on the cellular immune function of the rat under stress state]. Acupuncture Research 2002;27(3):211.
[38] . Zhao H, Du LN, Jiang JW, Wu GC, Cao XD. Neuroimmunal regulation of electroacupuncture (EA) on the traumatic rats. Acupunct Electrother Res 2002;27(1):15-27.
[39] . Li L, Yin-Xiang C, Hong X, Peng L, Da-Nian Z. Nitric oxide in vPAG mediates the depressor response to acupuncture in stress-induced hypertensive rats. Acupunct Electrother Res 2001;26(3):165-70.
[40] . Tjen ALSC, Li P, Longhurst JC. Prolonged inhibition of rostral ventral lateral medullary premotor sympathetic neurons by electroacupuncture in cats. Auton Neurosci 2003;106(2):119-31.
[41] . Guo ZL, Moazzami AR, Longhurst JC. Electroacupuncture induces c-Fos expression in the rostral ventrolateral medulla and periaqueductal gray in cats: relation to opioid containing neurons. Brain Res 2004;1030(1):103-15.
[42] . Chao DM, Shen LL, Tjen ALS, Pitsillides KF, Li P, Longhurst JC. Naloxone reverses inhibitory effect of electroacupuncture on sympathetic cardiovascular reflex responses. Am J Physiol 1999;276(6 Pt 2):H2127-34.
[43] . Stéphan JM. Acupuncture expérimentale, stress et axe neuro-endocrinien. Acupuncture & Moxibustion 2005;4(4),340-349