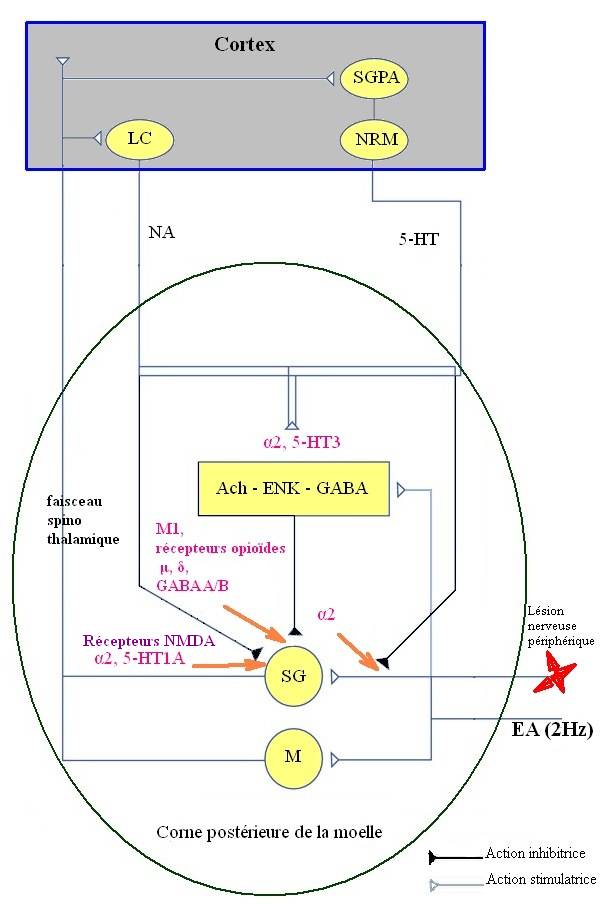
Résumé : Tout stress n’est pas forcément négatif. Le stress aigu est même nécessaire à nos réactions de survie et par extension à nos réactions d’excellence. En revanche, le stress chronique active au long cours l’axe neuro-endocrinien et le système limbique engendrant des pathologies psycho-somatiques non négligeables. L’acupuncture a un rôle à jouer et permettra de fixer de nouveaux objectifs pour transformer la vie du malade. L’acupuncture expérimentale offre des réponses physiopathologiques, en particulier son action inhibante de l’axe hypothalamo-hypophyso-surrénalien et son action stimulante du système limbique, le tout visualisable par localisation cérébrale de l’expression du proto-oncogène c-fos (gène de réponse précoce). Mots-clés : acupuncture expérimentale – revue – stress – CRH – ACTH – système limbique – interleukine – système nerveux sympathique – NPY – BDNF – c-fos – gène de réponse précoce
Summary : Any stress is not inevitably negative. The acute stress is even necessary to our reactions of survival and by extension to our reactions of excellence. On the other hand, chronic stress active with the long course the neuroendocrine axis and the limbic system generating of considerable psycho-somatic pathologies. Acupuncture has a role to play and will make it possible to lay down new objectives to transform the life of the patient. Experimental acupuncture offers physiopathological answers, in particular its action inhibiting of the hypothalamo-pituitary-adrenal axis and its stimulative action of the limbic system. It is visible by cerebral localization of the proto-oncogene c-fos expression ( immediate early gene). Keywords : experimental acupuncture – review – stress – CRH – ACTH – limbic system – interleukin – sympathetic nerve system – NPY – BDNF – c-fos – immediate early gene
L’acupuncture a une action non négligeable sur le stress. Ainsi, dans un essai clinique randomisé, l’équipe de Fassoulaki avait objectivé chez 25 patients que le point HM1 (yintang) le réduisait de manière statistiquement significative [1] . Dans un autre ECR tout récent, le même point yintang était stimulé avec succès chez les parents (p=0,03) dont l’anxiété était relative à l’attente d’une intervention chirurgicale chez leurs enfants [2] . L’action de l’acupuncture sur le stress permet de réduire l’activité du système nerveux sympathique et de ses cathécolamines [3] . L’axe hypothalamo-hypophyso-surrénalien n’est pas la seule cible de l’électroacupuncture. Nous verrons en autres que le système limbique participe également à son action.
Physiologie
Stress et action sur l’axe hypothalamo-hypophyso-surrénalien
En cas de stress, les catécholamines (adrénaline et noradrénaline) sont libérées en quelques secondes par les terminaisons du système nerveux orthosympathique et par les glandes médullo-surrénales. La CRH (corticotropin-releasing hormone), généralement considérée comme le principal médiateur hypothalamique de la réponse au stress déclenche une activation de l’axe hypothalamo-hypophyso-corticosurrénalien qui conduit à la libération d’ACTH et de glucocorticoïdes (cortisol). En plus de ces deux voies, l’activation de l’hypothalamus entraîne la libération par l’hypophyse d’hormone antidiurétique (ADH) ou vasopressine, de prolactine, de TSH, d’hormone de croissance, de bêta endorphines et une diminution de la sécrétion des hormones gonadotropes [4] , [5] . Libération aussi de VIP (Vasoactive Intestinal Peptide) qui est une neurohormone sécrétée par les terminaisons nerveuses. Ces différents médiateurs ont la capacité d’influencer les réactions immunitaires ou inflammatoires car d’importantes interconnexions existent entre la réaction endocrinienne et le système immunitaire, en particulier les cytokines (IL-1, IL-2, IL-6, TNF).
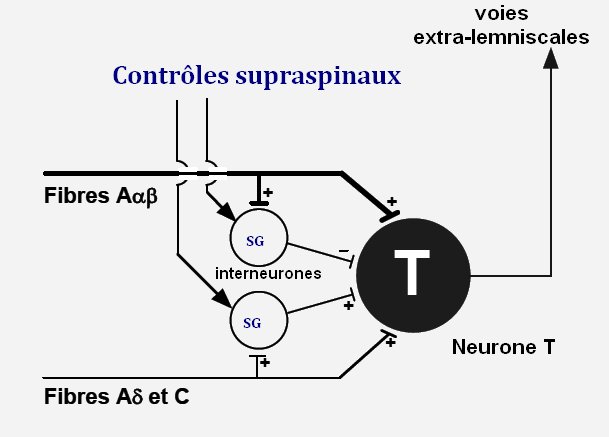
La figure 1 résume les différentes actions du stress sur le système hypothalamo-hypophyso-surrélanien et le système immunitaire.
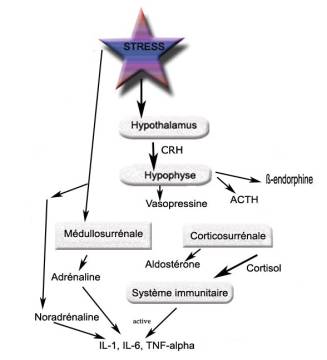
Figure 1. Principales actions du stress sur l’axe hypothalamo-hypophyso-surrénalien, le système immunitaire.
Stress et système limbique
Brain-derived neurotrophic factor (BDNF)
Les facteurs neurotrophiques constituent une famille de protéines stimulant la croissance, la différenciation et la survie de populations neuronales spécifiques. Le NGF découvert dans les années cinquante, est le chef de file de ces facteurs de croissance. Les facteurs neurotrophiques jouent bien sûr un rôle essentiel lors du développement, mais leur activité physiologique sur le système nerveux mature a été caractérisée plus récemment : dans plusieurs modèles-animaux de lésions et de maladies neurologiques, ils se sont avérés aptes à réguler le fonctionnement neuronal et à prévenir la mort neuronale. Dans l’hippocampe, le stress d’immobilisation diminue le niveau de l’ARNm du BDNF (brain-derived neurotrophic factor). De ce fait, on observe une atrophie et une mort des dendrites des neurones chez le rat. On a pu ainsi démontrer que cela était en rapport avec une diminution du taux de BDNF qui maintient la survie et la morphologie neuronale et joue donc un rôle dans la diminution du volume de l’hippocampe chez les personnes souffrant de stress chronique voire de maladies dépressives [6] .
Neuropeptide Y (NPY)
NPY est constitué de 36 acides aminés et se trouve présent dans le système nerveux central et le système nerveux autonome (fibres sympathiques où sa distribution suit celle de la noradrénaline). Sa libération au niveau de l’hypothalamus est augmentée pendant le jeûne, inhibée par la leptine et l’insuline et augmentée par les glucocorticoïdes. L’effet le plus notable du NPY est la stimulation de l’appétit par effet hypothalamique. Il diminue également la thermogenèse des adipocytes et favorise l’obésité. Le NPY a par ailleurs un effet anxiolytique et sédatif, un effet antinociceptif (analgésique). Il pourrait jouer un rôle dans la régulation centrale de la pression artérielle, car, injecté dans certaines zones du cerveau de l’animal, il provoque une hypotension et une bradycardie. Il pourrait inhiber la libération de certains médiateurs, celle du glutamate par exemple. Il favoriserait la sécrétion d’ACTH et inhiberait celle de la GH et de la TSH. Le neuropeptide Y (NPY) est bien connu pour améliorer le sommeil par ses propriétés anxiolytiques et sédatives en inhibant la libération d’ACTH et de cortisol [7] . Des événements stressants très tôt dans la vie, comme la privation maternelle chez le raton Wistar entraîne une diminution au niveau de l’hippocampe et du cortex occipital des taux de neuropeptide Y et de CGRP (calcitonin-gene related peptide) et suggèrent leur implication dans la réponse neuroendocrine au stress [8] .
Stress et gène de réponse précoce
C-fos
Les proto-oncogènes sont des gènes qui sont transcrits pour produire des facteurs intervenant dans la transduction des signaux cellulaires. L’un d’eux, le c-fos est une protéine de 380 acides aminés présente sur le chromosome 14 des cellules eucaryotes et correspond à un facteur de transcription. Son action modifie le signal normalement exprimé par la cellule. Les facteurs de transcription génique sont des protéines nucléaires dont la fonction est d’induire la réplication d’un gène. Constitutionnels, leur activité biochimique est alors induite le plus souvent par leur phosphorylation ou leur liaison à une autre protéine. Inductibles, leur synthèse est alors provoquée par un second messager. Ces protéines se combinent entre elles, forment souvent des dimères et se lient ensuite à un site dit promoteur sur un gène cible. Le site promoteur, une fois activé, est le point de départ de la réplication du gène cible par la RNA polymérase. La production de RNA messager est suivie de sa translocation dans le cytoplasme et de sa traduction en une protéine. Chaque facteur de transcription a une activité induite par un signal donné par le biais d’un système de second messager. Un facteur de transcription assure ainsi le lien entre ce signal et la régulation de l’expression du génome.
Le facteur de transcription le plus fréquemment synthétisé dans une cellule après un signal activateur est c-fos. Les facteurs les plus dimérisables avec c-fos appartiennent à la famille jun comme le c-jun, inductibles ou activables. Le site promoteur reconnaissant électivement les dimères fos/jun et régulant de nombreux gènes de fonction est le site AP1. L’activité c-Fos est généralement extrêmement faible dans la plupart des tissus adultes non stimulés [9] , mais peut être augmentée de façon spectaculaire par de nombreux signaux comme le stress et les facteurs de croissance [10] , les irradiations UV ou l’H2O2 [11] , les stimulations mécaniques [12] etc.. Dans le cerveau, le niveau basal est faible et limité mais lors d’une stimulation comme par exemple un agent épileptogène, on observe une induction forte et générale, dans presque tout le cerveau [13] . L’activation de l’expression de c-fos par toutes sortes de stimuli est rapide mais aussi très brève car le temps maximum d’accumulation de messager est d’environ 30 minutes après stimulation et 60 minutes pour la protéine. C-fos est considéré comme un gène de réponse précoce (Immediate Early Genes, IEG). Cette fenêtre d’expression étroite temporellement suggère que c-fos subisse un contrôle très strict à plusieurs niveaux [14] . En effet, l’expression et l’activité de c-fos sont réglées à de multiples niveaux du démarrage de la transcription à l’allongement du messager jusqu’à la stabilité et la modification de la protéine. La transcription du c-fos et son élongation sont ainsi sous le contrôle du calcium cellulaire et de l’ARN polymérase II.
Une réduction du flux sanguin cérébral sans destruction des tissus, comme on l’observe dans les migraines, induite expérimentalement chez la souris a permis ainsi de constater que l’expression de c-fos était localisée dans les neurones des régions associées à la réponse au stress et l’immunomodulation tels la substance grise périaqueducale du mésencéphale et les noyaux périventriculaires [15] .
Localisation cérébrale de l’expression c-fos relative au stress chez les animaux
Des rats en état de stress par immobilisation de 60 mn par jour pendant 10 jours montrent des altérations de leur état avec tachycardie, hypothermie transitoire, élévation importante du taux de corticostérone, surtout lors de la première séance, s’atténuant légèrement au cours des autres séances de stress tout en restant encore élevé. Comparativement à des rats non immobilisés, on observe 60 minutes après la fin de la première séance chez les rats stressés une élévation de l’expression du c-fos au niveau du noyau paraventriculaire hypothalamique, du septum latéral de l’hypothalamus, de l’aire latérale préoptique, l’aire latérale hypothalamique, l’amygdale médiale, le locus coeruleus et dans une structure du tronc cérébral (noyau de Barrington). 60 minutes après la 10ème séance de stress, l’expression de c-fos est diminuée nettement dans certains de ces secteurs comparés au modèle observé après la première séance, surtout au niveau du noyau paraventriculaire dans les régions des neurones parvocellulaires dorsale et médiale et dans l’amygdale médiale. A noter que le noyau paraventriculaire hypothalamique (PVN) contient deux types de cellules : – parvocellulaire médiale qui sécrète la CRH (corticotropin-releasing hormone) ; parvocellulaire dorsale et ventriculaire possédant des neurones se projetant vers le tronc cérébral et la moëlle épinière (exercent un contrôle du système autonome), et certains neurones sécrètent l’ocytocine et la vasopressine ; – cellules magnocellulaires contrôlant la sécrétion l’ocytocine et la vasopressine directement en rapport avec l’hypophyse postérieure. Cependant, dans tous les autres secteurs mesurés, l’augmentation de c-fos était présente même après des stress répétés. Ces résultats prouvent que les réponses neuronales et physiologiques s’adaptent à un stress répété, mais que dans tous les cas, il y a des éléments fortement spécifiques. Il existe une régulation des systèmes autonome et endocrine par l’intermédiaire du noyau paraventriculaire hypothalamique impliquée dans la régulation des corticoïdes [16] .
Un autre travail confirme ces résultats lors du stress, avec élévation de l’expression du c-fos dans le noyau des neurones du septum latéral et le noyau médial du thalamus, mais surtout dans le noyau paraventriculaire hypothalamique (régions à neurones parvocellulaires dorso-médiale) et les neurones cathécolaminergiques et sérotoninergiques du tronc cérébral [17] . Une autre étude montre que l’expression c-fos est activée 2 heures après le stress principalement au niveau du PVN correspondant aux neurones synthétisant la CRH et secondairement au niveau des neurones mésencéphaliques du raphé magnus ocytocinergique, dans la région limbique, le tegmentum ainsi que dans les projections de cellules cathécholaminergiques médullaires [18] . 30 à 60 minutes après un stress d’immobilisation, on observe chez le rat l’induction d’ARNm de c-fos au niveau du noyau latéral du septum, du noyau paraventriculaire hypothalamique, du noyau dorso médial hypothalamique, le noyau antérieur hypothalamique, la portion latérale de l’aire rétrochiasmatique, les noyaux amygdaliens cortical et médial, la substance grise périaqueducale et le locus coeruleus riche en neurones noradrénergiques [19] . Une localisation quasi similaire avec mise en évidence de l’activation du système autonome noradrénergique et du système hypothalamo-hypophysaire surrénalien en réponse au stress par l’induction de c-fos au niveau du noyau paraventriculaire hypothalamique, du locus coeruleus, des noyaux amygdalien central et médial, du noyau du lit de la strie terminale a été objectivé chez les rats Sprague-Dawley [20] .
Toujours chez le rat, un stress par immobilisation dans des tubes de plexiglas mène à l’augmentation du CRH, de l’ACTH, de la corticostérone par activation de l’axe hypothalamo-hypophyso-surrénalien visualisée par une élévation de l’expression de l’ARNm du c-fos dans le cortex, l’hippocampe, l’hypothalamus, le septum, l’amygdale et le tronc cérébral (voir figures 2,3,4). Cependant, l’exposition répétée à ce même stress pendant 9 jours a généralement pour conséquence une accoutumance avec régression de l’expression de l’ARNm c-fos, en rapport avec la régulation de la corticostérone afférente à cet axe, mais aussi par régulation de l’expression du c-fos par d’autres molécules informationnelles telles les cytokines (IL-6), ou les facteurs de croissance comme l’EGF (epidermal growth factor) ou le NGF (nerve growth factor) [21] . Un travail similaire sur le stress par immobilisation retrouve au bout de 10 jours une diminuation des réponses de l’axe hypothalamo-hypophyso-surrénalien et des neurones cathélolaminergiques du locus coeruleus [22] .
Chez le lapin, un stress d’immobilisation entraîne lors du premier jour une altération au niveau du noyau arqué périventriculaire et ventro-médial de l’hypothalamus, la strie terminale de l’amygdale et le fornix dorsal de l’hippocampe, mais ces réponses disparaissent au 7è jour [23] .
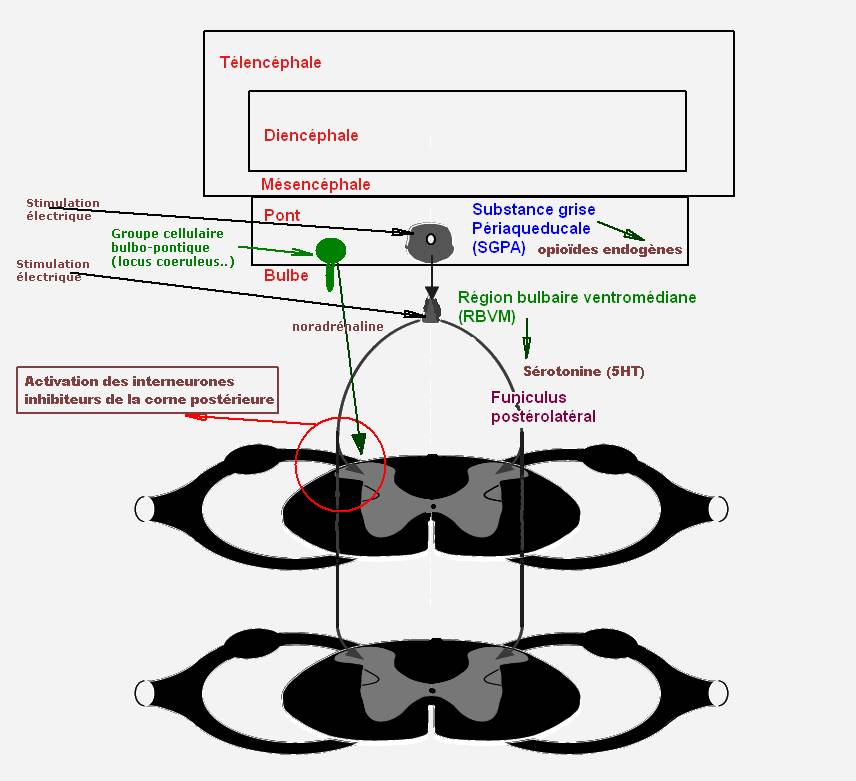
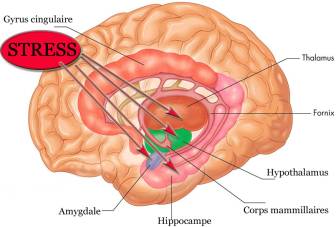 Figure 2. Principales structures intervenant dans la réponse au stress. Figure 2. Principales structures intervenant dans la réponse au stress. | 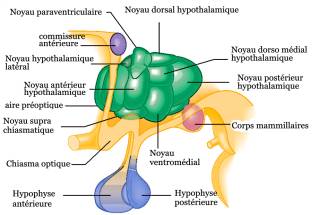 Figure 3. Stress et noyaux hypothalamiques, hypophyse |
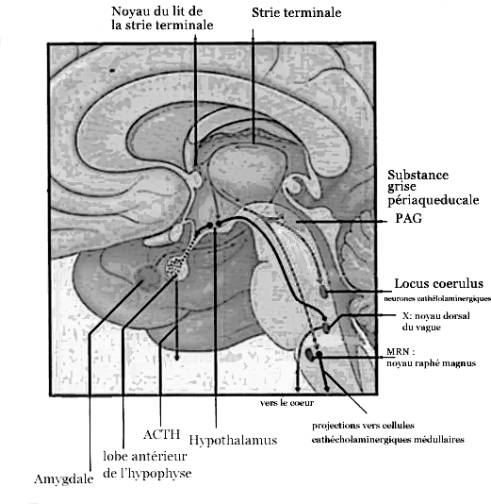 Figure 4. Stress et système limbique, axe hypothalamo-hypophysaire corticotrope et les efférences de l’amygdale passant par la strie terminale activant le système autonome noradrénergique. |
Action de l’acupuncture sur le stress
Axe hypothalo-hypophyso-surrénalien et adrénergique
En 1980, Liao et coll. ont montré chez le lapin exposé à trois variétés de stress (stress d’immobilisation, exposition à la chaleur ou au froid) que l’électroacupuncture appliquée au point ES36 (zusanli) inhibait l’hypersécrétion des hormones glucocorticoïdes (cortisol et corticostérone) [24] .
Chez le rat anesthésié, la stimulation électrique à basse fréquence du zusanli (ES36) ou la stimulation thermique nociceptive provoquée en immergeant la patte dans l’eau à 52°C entraîne une expression de c-fos dans le lobe antérieur de la glande hypophysaire, aussi bien qu’au niveau des noyaux hypothalamiques arqués et autres noyaux voisins. Une réponse semblable du lobe antérieur fut provoquée par un stress d’immobilisation chez les rats non anesthésiés, mais dans ce cas, les cellules c-fos immunoréactives étaient visibles jusqu’au lobe intermédiaire et étaient même très abondantes dans le noyau paraventriculaire hypothalamique. Les auteurs suggéraient que les cellules pituitaires antérieures qui répondent au stress sont également activées par l’acupuncture ou par stimulation douloureuse. Cependant, les mécanismes de l’activation de l’hypophyse semblent distincts dans le stress, puisque les différents noyaux hypothalamiques sont impliqués [25] avec une spécificité de localisation lors de la nociception au niveau du noyau hypothalamique médio-basal et arqué, et moins dans le noyau paraventriculaire qui sera davantage activé lors de l’action de l’électroacupuncture dans le stress [26] . De ce fait, l’électroacupuncture utilisée chez le rat stressé module l’activité de l’axe hypothalamo-hypophyso-surrénalien [27] .
Guimares et al. en 1997 montraient que l’acupuncture aux points ES36, RM17, DU20, RP6, MC6 entraînait un effet anxiolytique chez le rat chez qui on induisait un stress d’immobilisation de 60 minutes, en rapport avec une diminution de 60% en moyenne (p<0,02) de la pression sanguine, du rythme cardiaque et des niveaux plasmatiques de corticostérone, adrénaline et noradrénaline [28] .
Chez des rats dont la dépression a été induite par un stress chronique, on a observé les effets des points 20VG (baihui) et 6RA (sanyinjiao) sur les taux plasmatiques du cortisol et de l’hormone ACTH. A été aussi mesuré quantitativement le nombre des neurones à vasopressine du noyau paraventriculaire hypothalamique (la vasopressine ou ADH est synthétisée au niveau de l’hypothalamus, transportée puis stockée dans la post-hypophyse qui la libère dans la circulation sanguine). Les résultats montrent que les taux de cortisol et d’ACTH plasmatiques ainsi que le nombre de neurones à vasopressine du noyau paraventriculaire hypothalamique étaient évidemment plus élevés dans le groupe stress que dans le groupe témoin, mais statistiquement abaissés dans le groupe électroacupuncture par rapport au groupe stress sans acupuncture. L’étude suggère que la régulation de l’hyperactivité des fonctions de l’axe hypothalamo-hypophyso-surrénalien est un des mécanismes du traitement de la dépression par électroacupuncture [29] .
L’immobilisation forcée est un facteur simple et efficace de stress qui entraîne une tachycardie, une hypertension artérielle et une élévation plasmatique de la norépinéphrine (noradrénaline) et de l’épinéphrine (adrénaline). Cette étude a étudié les effets de l’électroacupuncture chez les rats subissant un stress d’immobilisation. Les rats mâles Sprague-Dawley ont bénéficié d’électroacupuncture (3 hertz, 20 mA) pendant 30 minutes après le début du stress d’immobilisation (180 minutes). L’électroacupuncture des points 3CO (shaohai) et MC6 (neiguan) réduit de manière statistiquement significative toutes les variables étudiées, en particulier l’adrénaline et la noradrénaline 3 heures après le stress d’immobilisation. Mais l’électroacupuncture délivrée sur des non-points (à la queue) ou aux points GI11 (quchi) et TR5 (waiguan) n’a aucun effet [30] .
Lee et coll avaient déjà étudié l’action de l’électroacupuncture (EA) sur les points 3CO (shaohai) et 6MC (neiguan) qui atténuent les réponses périphériques stress-induites, incluant l’augmentation de la pression sanguine, la tachycardie et l’élévation des cathécolamines plasmatiques. Dans cette nouvelle étude, ils ont examiné l’effet central de l’EA sur l’expression de c-fos dans le cerveau des rats soumis à un stress d’immobilisation (180 minutes). Celui-ci produit préférentiellement une augmentation significative du c-fos dans le noyau paraventriculaire hypothalamique (PVN), le noyau arqué (ARN), le noyau supraoptique (SON), le noyau suprachiasmatique (SCN), le noyau médial amygdaloïde (AME), le noyau du lit de la strie terminale (BST), l’hippocampe, le septum latéral (LS), le noyau accumbens et le locus coeruleus (LC). L’EA (3 hertz, 20 mA) sur les points 3CO (shaohai) et 6MC (neiguan) pendant 30 minutes durant le stress atténue significativement l’expression de c-fos dans la région parvocellulaire du PVN, SON, SCN, AME, LS et LC. Cependant, l’EA n’a entraîné aucun effet sur l’expression c-fos dans la région magnocellulaire du PVN, ARN, BST ou l’hippocampe. La stimulation électroacupuncturale sur 3CO et sur 6MC a eu davantage d’effet inhibiteur sur l’expression c-fos provoquée par le stress que l’EA réalisée sur le TR5 et 11GI ou des non-acupoints [31] .
Le système limbique
Le stress induit une atrophie et une mort neuronale spécialement dans l’hippocampe. En effet, les altérations dans l’expression des facteurs neurotrophiques ont été impliquées dans la dégénérescence hippocampale stress-induite. L’objectif de ce travail a été de voir si l’électroacupuncture appliquée sur le ES36 (zusanli) peut influencer l’expression de la BDNF dans l’hippocampe d’un groupe de rats exposés à un stress d’immobilisation dans des sacs en plastique. Après traitement, les rats étaient décapités et l’hippocampe rapidement enlevée. L’analyse de la réaction de polymérase et l’isolation de la transcription de l’ARN montrait que la stimulation électroacupuncturale restaurait de manière statistiquement significative l’expression de l’ARNm du BDNF chez les rats soumis à un stress d’immobilisation [32] .
La séparation maternelle est un facteur de risque dans le développement des désordres de l’humeur comme la dépression. Les études sur animaux ou êtres humains objectivent la participation du neuropeptide Y (NPY). Pour étudier l’effet de l’acupuncture sur la dépression et examiner des changements de l’expression de NPY liés à la séparation maternelle, les auteurs ont mesuré le poids corporel et l’activité locomotrice, et analysé par immunohistochimie l’expression de la NPY dans l’hippocampe. La séparation maternelle pendant 7 jours commençant le 14è jour postnatal induit une diminution significative de poids corporel et de la locomotion, alors que le traitement acupunctural au 7CO (shenmen) entraîne une augmentation significative des deux. L’immunoréactivité des neurones à NPY est diminuée dans l’aire CA1 et le gyrus dentelé (un des trois éléments constitutifs de l’hippocampe avec la corne d’Ammon et le subiculum) pour le groupe de rats avec séparation maternelle, mais significativement augmentée dans le groupe d’acupuncture. Ces résultats suggèrent que l’acupuncture a un effet sur les désordres apparentés à la dépression, probablement en modulant l’expression de NPY dans l’hippocampe [33] .
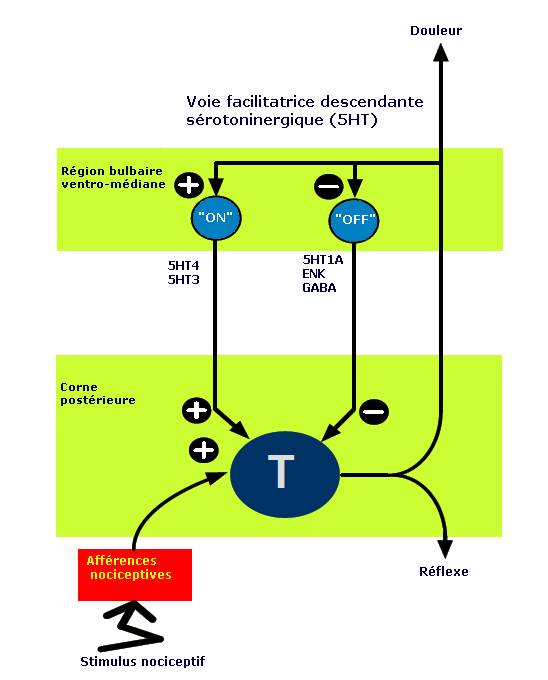
Des ratons femelles Wistar ont été séparés de leurs mères 3h quotidiennement du 3ème jour postnatal au 14ème jour. Des groupes d’acupuncture ont été traités par le point shenmen (7CO) ou zusanli (ES36) alternativement du 50ème jour au 62ème jour postnatal. Le nombre de cellules de NPY-immunoréactives localisées au niveau de l’amygdale baso-latérale (BLA) était inférieur dans le groupe (SM) des rats séparés de leur mère comparé au groupe contrôle. Parmi les groupes maternellement séparés, le nombre de cellules NPY-immunoréactives dans le BLA était statistiquement plus élevé dans le groupe acupuncture-7CO, mais pas plus élevé dans le groupe acupuncture-ES36, le tout comparativement au groupe SM. Ces résultats suggèrent que le traitement acupunctural pourrait réduire l’anxiété comportementale chez des rats devenus adultes ayant été séparés maternellement en modulant le système du NPY dans l’amygdale [34] . La figure 5 résume l’action de l’acupuncture sur l’axe neuro-endocrine et le système limbique.
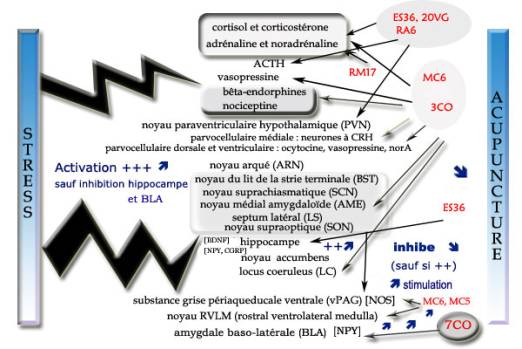
Figure 5. Effets de l’acupuncture sur l’axe neuro-endocrine et le système limbique.
Paradigme du stress animal : application à l’acupuncture expérimentale
Chez les animaux de laboratoire, l’acupuncture doit être exécutée sur des sujets anesthésiés ou, s’ils ne le sont pas, sur des sujets immobilisés. Or ces deux procédures induisent un changement de l’expression de l’activité c-fos au niveau cérébral et peuvent ainsi masquer la réponse spécifique de l’expression c-fos par électroacupuncture. De ce fait, afin de réduire les effets du stress d’immobilisation, les auteurs ont proposé un protocole de stress répété pour évaluer les régions cérébrales activées par électroacupuncture chez des rats mâles adultes Wistar. Les protocoles d’immobilisation répétée (6 jours, 1 h/jour et 13 jours, 2 h/jour) ont été employés pour réduire l’effet du stress aigu d’immobilisation et visualiser ainsi l’expression c-fos réellement induite par électroacupuncture au point ES36 (zusanli). Des animaux soumis seulement à l’immobilisation (dans un cylindre en plastique) ou soumis à l’électroacupuncture (100 hertz) sur un non-point d’acupuncture ont été comparés aux animaux immobilisés et soumis à l’électroacupuncture à l’ES36. L’expression c-fos a été mesurée sur 41 secteurs du cerveau. Les protocoles de l’immobilisation répétée ont réduit de manière statistiquement significative l’expression c-fos immobilisation-induite dans la plupart des secteurs de cerveau analysés (p<0,05). Les animaux traités par EA sur ES36 ont eu des niveaux sensiblement plus élevés de l’expression c-fos dans le noyau dorsal du raphé, dans le locus coeruleus, dans l’hypothalamus postérieur et dans le noyau médio-central du thalamus. En outre, les protocoles répétés d’immobilisation ont intensifié les différences entre les effets de ES36 et la stimulation des non-points acupuncturaux dans le noyau dorsal du raphé (p<0,05). Ces données suggèrent que des niveaux élevés de stress peuvent interagir et masquer l’évaluation des effets spécifiques de l’acupuncture chez les animaux non anesthésiés, d’où l’intérêt pour connaître l’efficacité d’un point d’acupuncture d’utiliser des animaux immobilisés pendant 13 jours. Cela aura pour effet de diminuer très fortement l’expression c-fos induite par le stress d’immobilisation et de connaître le lieu exact de l’expression c-fos spécifique de l’activité acupuncturale recherchée [35] .
De la même façon, les effets de l’électroacupuncture dans l’addiction aux opiacés sont partiellement masqués par le stress d’immobilisation. En effet, il est difficile de réaliser l’électroacupuncture sur les quatre membres des animaux non immobilisés. D’où, il a été évalué chez des rats libres de leurs mouvements et d’autres immobilisés, l’effet de l’électroacupuncture au point V23 (shenshu) dans le sevrage à la morphine et l’expression du c-fos au niveau de l’amygdale. Le taux de corticostérone a été dosé ainsi que les réponses comportementales durant la stimulation électroacupuncturale de 100 Hz pendant 30 mn. Dans les deux groupes de rats, l’électroacupuncture réduit significativement les signes de sevrage. L’EA atténue chez les rats libres l’expression du c-fos dans le noyau central de l’amygdale tandis que l’EA chez les rats immobilisés augmente la réponse. La corticostérone est significativement plus élevée chez les animaux immobilisés après stimulation par EA [36] .
En définitive, le stress avec son cortège de réponses de l’organisme, variable en intensité selon la nature de ce stimulus ou sa durée d’application dans le temps peut parfaitement être canalisé par l’acupuncture. L’acupuncture expérimentale explique l’action cybernétique des points qui agissent aussi bien sur l’axe hypothalamo-hypophyso-surrénalien et la libération principale de CRH (corticotropin-releasing hormone) que sur la mise en jeu des phénomènes de transduction avec ses nombreuses molécules informationnelles que nous développerons dans un prochain article. De ce fait, l’acupuncture a un rôle essentiel à jouer dans la médecine moderne occidentale et doit absolument trouver sa place dans la panoplie thérapeutique.

Références
[1] . Fassoulaki A, Paraskeva A, Patris K, Pourgiezi T, Kostopanagiotou G. Pressure applied on the extra 1 acupuncture point reduces bispectral index values and stress in volunteers. Anesth Analg 2003;96(3):885-90, table of contents.
[2] . Wang SM, Gaal D, Maranets I, Caldwell-Andrews A, Kain ZN. Acupressure and preoperative parental anxiety: a pilot study. Anesth Analg 2005;101(3):666-9.
[3] . Middlekauff HR, Hui K, Yu JL, Hamilton MA, Fonarow GC, Moriguchi J, et al. Acupuncture inhibits sympathetic activation during mental stress in advanced heart failure patients. J Card Fail 2002;8(6):399-406.
[4] . Slominski A, Wortsman J, Luger T, Paus R, Solomon S. Corticotropin releasing hormone and proopiomelanocortin involvement in the cutaneous response to stress. Physiol Rev 2000;80(3):979-1020.
[5] . Jessop DS, Douthwaite JA, Conde GL, Lightman SL, Dayan CM, Harbuz MS. Effects of Acute Stress or Centrally Injected Interleukin-1beta on Neuropeptide Expression in the Immune System. Stress 1997;2(2):133-144.
[6] . Murakami S, Imbe H, Morikawa Y, Kubo C, Senba E. Chronic stress, as well as acute stress, reduces BDNF mRNA expression in the rat hippocampus but less robustly. Neurosci Res 2005.
[7] . Antonijevic IA, Murck H, Bohlhalter S, Frieboes RM, Holsboer F, Steiger A. Neuropeptide Y promotes sleep and inhibits ACTH and cortisol release in young men. Neuropharmacology 2000;39(8):1474-81.
[8] . Husum H, Termeer E, Mathe AA, Bolwig TG, Ellenbroek BA. Early maternal deprivation alters hippocampal levels of neuropeptide Y and calcitonin-gene related peptide in adult rats. Neuropharmacology 2002;42(6):798-806.
[9] . Piechaczyk M, Blanchard JM. c-fos proto-oncogene regulation and function. Crit Rev Oncol Hematol 1994;17(2):93-131.
[10] . Muller R, Bravo R, Burckhardt J, Curran T. Induction of c-fos gene and protein by growth factors precedes activation of c-myc. Nature 1984;312(5996):716-20.
[11] . Devary Y, Gottlieb RA, Lau LF, Karin M. Rapid and preferential activation of the c-jun gene during the mammalian UV response. Mol Cell Biol 1991;11(5):2804-11.
[12] . Sadoshima J, Izumo S. Mechanical stretch rapidly activates multiple signal transduction pathways in cardiac myocytes: potential involvement of an autocrine/paracrine mechanism. Embo J 1993;12(4):1681-92.
[13] . Smeyne RJ, Schilling K, Robertson L, Luk D, Oberdick J, Curran T, et al. fos-lacZ transgenic mice: mapping sites of gene induction in the central nervous system. Neuron 1992;8(1):13-23.
[14] . Coulon V. Régulation intragénique de la transcription de c-fos : blocage de l’élongation et promoteur alterne. Montpellier: Université Montpellier II, Sciences et Techniques du Languedoc UFR Sciences; 2001.
[15] . Liverman CS, Cui L, Yong C, Choudhuri R, Klein RM, Welch KM, et al. Response of the brain to oligemia: gene expression, c-Fos, and Nrf2 localization. Brain Res Mol Brain Res 2004;126(1):57-66.
[16] . Chen X, Herbert J. Regional changes in c-fos expression in the basal forebrain and brainstem during adaptation to repeated stress: correlations with cardiovascular, hypothermic and endocrine responses. Neuroscience 1995;64(3):675-85.
[17] . Senba E, Matsunaga K, Tohyama M, Noguchi K. Stress-induced c-fos expression in the rat brain: activation mechanism of sympathetic pathway. Brain Res Bull 1993;31(3-4):329-44.
[18] . Li HY, Sawchenko PE. Hypothalamic effector neurons and extended circuitries activated in « neurogenic » stress: a comparison of footshock effects exerted acutely, chronically, and in animals with controlled glucocorticoid levels. J Comp Neurol 1998;393(2):244-66.
[19] . Cullinan WE, Herman JP, Battaglia DF, Akil H, Watson SJ. Pattern and time course of immediate early gene expression in rat brain following acute stress. Neuroscience 1995;64(2):477-505.
[20] . Ma S, Morilak DA. Induction of FOS expression by acute immobilization stress is reduced in locus coeruleus and medial amygdala of Wistar-Kyoto rats compared to Sprague-Dawley rats. Neuroscience 2004;124(4):963-72.
[21] . Melia KR, Ryabinin AE, Schroeder R, Bloom FE, Wilson MC. Induction and habituation of immediate early gene expression in rat brain by acute and repeated restraint stress. J Neurosci 1994;14(10):5929-38.
[22] . Lachuer J, Delton I, Buda M, Tappaz M. The habituation of brainstem catecholaminergic groups to chronic daily restraint stress is stress specific like that of the hypothalamo-pituitary-adrenal axis. Brain Res 1994;638(1-2):196-202.
[23] . Seto K, Liao YY, Saito H, Edashige N, Kawakami M. Influence of lesions in the limbic-hypothalamic system on metabolic response of acetate to daily repeated immobilization stress. Exp Clin Endocrinol 1984;83(1):37-48.
[24] . Liao YY, Seto K, Saito H, Fujita M, Kawakami M. Effects of acupuncture on adrenocortical hormone production. (II) Effect of acupuncture on the response of adrenocortical hormone production to stress. Am J Chin Med 1980;8(1-2):160-6.
[25] . Pan B, Castro-Lopes JM, Coimbra A. C-fos expression in the hypothalamo-pituitary system induced by electroacupuncture or noxious stimulation. Neuroreport 1994;5(13):1649-52.
[26] . Pan B, Castro-Lopes JM, Coimbra A. Activation of anterior lobe corticotrophs by electroacupuncture or noxious stimulation in the anaesthetized rat, as shown by colocalization of Fos protein with ACTH and beta-endorphin and increased hormone release. Brain Res Bull 1996;40(3):175-82.
[27] . Pan B, Castro-Lopes JM, Coimbra A. Chemical sensory deafferentation abolishes hypothalamic pituitary activation induced by noxious stimulation or electroacupuncture but only decreases that caused by immobilization stress. A c-fos study. Neuroscience 1997;78(4):1059-68.
[28] . Guimaraes CM, Pinge MC, Yamamura Y, Mello LE. Effects of acupuncture on behavioral, cardiovascular and hormonal responses in restraint-stressed Wistar rats. Braz J Med Biol Res 1997;30(12):1445-50.
[29] . Cui H, Xiahong L, Xuewu L et Al. [Effects of puncturing the acupoints of baihui and sanyinjiao by electric needles on the HPA axis in the rat chronic stress-induced depression model]. Journal of Beijing University of traditional chinese medecine 2001;24(3):74.
[30] . Yang CH, Lee BB, Jung HS, Shim I, Roh PU, Golden GT. Effect of electroacupuncture on response to immobilization stress. Pharmacol Biochem Behav 2002;72(4):847-55.
[31] . Lee HJ, Lee B, Choi SH, Hahm DH, Kim MR, Roh PU, et al. Electroacupuncture reduces stress-induced expression of c-fos in the brain of the rat. Am J Chin Med 2004;32(5):795-806.
[32] . Yun SJ, Park HJ, Yeom MJ, Hahm DH, Lee HJ, Lee EH. Effect of electroacupuncture on the stress-induced changes in brain-derived neurotrophic factor expression in rat hippocampus. Neurosci Lett 2002;318(2):85-8.
[33] . Lim S, Ryu YH, Kim ST, Hong MS, Park HJ. Acupuncture increases neuropeptide Y expression in hippocampus of maternally-separated rats. Neurosci Lett 2003;343(1):49-52.
[34] . Park HJ, Chae Y, Jang J, Shim I, Lee H, Lim S. The effect of acupuncture on anxiety and neuropeptide Y expression in the basolateral amygdala of maternally separated rats. Neurosci Lett 2005;377(3):179-84.
[35] . Medeiros MA, Canteras NS, Suchecki D, Mello LE. c-Fos expression induced by electroacupuncture at the Zusanli point in rats submitted to repeated immobilization. Braz J Med Biol Res 2003;36(12):1673-84.
[36] . Liu S, Zhou W, Liu H, Yang G, Zhao W. Electroacupuncture attenuates morphine withdrawal signs and c-Fos expression in the central nucleus of the amygdala in freely moving rats. Brain Res 2005;1044(2):155-63.